Статья: Электропроводность щелочных растворов вольфрамата натрия
Статья: Электропроводность щелочных растворов вольфрамата натрия
Студ. Гадиев Г.А., студ.
Касаева М.С., доц. Алкацева В.М.
Кафедра металлургии цветных
металлов.
Северо-Кавказский
государственный технологический университет
Целью
работы явилось исследование зависимости удельной электропроводности щелочных
растворов вольфрамата натрия от их состава (WO3, NaOH) и температуры, а также
поиск условий, отвечающих их наибольшей удельной электропроводности.
Исследования
проводили на растворах с составом, близким к растворам, получаемым в результате
электрохимического растворения вторичного вольфрамового сырья.
Измерения
электропроводности растворов проводили с помощью переменно-токового
кондуктометра ОК-102/1 с платинированными электродами.
Как
показал предварительный анализ литературных данных [1-3], растворы, получаемые
электрохимическим растворением вторичного вольфрамового сырья, содержат до 120
г/дм3 WO3, 20-200 г/дм3 NaOH, а температура их находится в пределах 40-70 оС.
Несколько расширив эти границы, мы провели исследования на растворах состава
10-150 г/дм3 WO3 и 20-200 г/дм3 NaOH при температурах 20-70 оС, использовав планируемый
эксперимент.
Исходя
из этого, приняты следующие уровни независимых переменных:
WO3,
г/л 10 – 80 – 150;
NaOH,
г/л 20 – 110 – 200;
t,
оС 20 – 45 – 70.
Значения
независимых переменных в кодовом масштабе:
X1
= 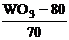 ; X2 = ; X2 = 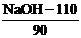 ; X3 = ; X3 = 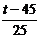 . (1) . (1)
Для
изучения электропроводности щелочных растворов вольфрамата натрия
воспользовались планом Рехтшафнера. Матрица планирования приведена в табл.1.
Растворы,
соответствующие по составу каждому пункту плана, готовили из однокомпонентных
растворов Na2WO4 и NaOH, которые в свою очередь были приготовлены из реактивов
марки ЧДА и ХЧ соответственно.
В
соответствии с составами растворов (табл.1) готовили в каждом случае 200 мл
раствора, содержащего Na2WO4 и NaOH. Приготовленный щелочной раствор
вольфрамата натрия переводили в стакан и замеряли электропроводность в
интервале температур 20-70 оС с шагом 5о. Поскольку составы растворов в
некоторых пунктах плана одинаковы, то при замере электропроводности их
объединили.
Пересчет
показаний кондуктометра (S) на удельную электропроводность проводили по формуле
c = 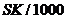 , См/м, (2) , См/м, (2)
где
К – постоянная ячейки.
Т
а б л и ц а 1
Матрица
планирования и результаты опытов
| № |
Кодовый масштаб |
Натуральный масштаб |
c, |
| оп. |
X1 |
X2 |
X3 |
WO3,
г/л
|
NaOH,
г/л
|
t,
оС
|
См/м |
| 1 |
- |
- |
- |
10 |
20 |
20 |
9,979 |
| 2 |
- |
+ |
+ |
10 |
200 |
70 |
61,948 |
| 3 |
+ |
- |
+ |
150 |
20 |
70 |
24,592 |
| 4 |
+ |
+ |
- |
150 |
200 |
20 |
21,796 |
| 5 |
- |
- |
+ |
10 |
20 |
70 |
18,800 |
| 6 |
- |
+ |
- |
10 |
200 |
20 |
29,581 |
| 7 |
+ |
- |
- |
150 |
20 |
20 |
12,207 |
| 8 |
+ |
0 |
0 |
150 |
110 |
45 |
36,887 |
| 9 |
0 |
+ |
0 |
80 |
200 |
45 |
43,192 |
| 10 |
0 |
0 |
+ |
80 |
110 |
70 |
51,031 |
| 11 |
0 |
0 |
0 |
80 |
110 |
45 |
38,759 |
Значения
удельной электропроводности растворов при 20-70 оС приведены в табл.2.
Обработкой
экспериментальных данных, представленных в табл.1, получена кодовая модель
зависимости удельной электропроводности щелочных растворов вольфрамата натрия
от состава и температуры:
c =
38,788 – 0,4891 X1 + 13,1934 X2 + 11,1972 X3 – 1,4269 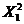 - -
-
8,8044 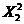 + 1,0309 + 1,0309 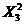 - 2,4959 X1X2 + 0,8983 X1X3 + - 2,4959 X1X2 + 0,8983 X1X3 +
+
5,8938 X2X3; (3)
Fрасч
= 130740,15; F0,05;10;1 = 242.
Т
а б л и ц а 2
Значения
удельной электропроводности растворов
при
20-70 оС, См/м
|
t,
oC
|
№ опыта |
| 1, 5 |
2, 6 |
3, 7 |
4 |
8 |
9 |
10, 11 |
| 20 |
9,979 |
29,581 |
12,207 |
21,796 |
24,324 |
25,942 |
26,463 |
| 25 |
10,870 |
32,700 |
13,454 |
25,006 |
26,641 |
28,616 |
29,047 |
| 30 |
11,672 |
35,818 |
14,612 |
28,750 |
29,225 |
32,494 |
31,631 |
| 35 |
12,563 |
39,204 |
15,771 |
32,360 |
31,809 |
36,104 |
34,125 |
| 40 |
13,543 |
42,501 |
17,107 |
35,703 |
34,304 |
39,849 |
36,531 |
| 45 |
14,345 |
45,849 |
18,266 |
39,315 |
36,887 |
43,192 |
38,759 |
| 50 |
15,236 |
49,327 |
19,602 |
42,657 |
38,937 |
46,401 |
41,432 |
| 55 |
16,038 |
52,417 |
21,028 |
45,866 |
41,877 |
49,878 |
43,926 |
| 60 |
16,929 |
55,766 |
22,275 |
50,011 |
44,105 |
53,087 |
46,252 |
| 65 |
17,820 |
58,857 |
23,522 |
52,953 |
46,647 |
56,430 |
48,835 |
| 70 |
18,800 |
61,948 |
24,592 |
55,360 |
48,807 |
59,372 |
51,031 |
Поскольку
чем выше удельная электропроводность раствора, тем ниже удельный расход
электроэнергии на электрохимическое растворение вторичного вольфрамового сырья,
то методом нелинейного программирования по модели (3) был найден максимум
целевой функции c
= 62,062 См/м и его координаты:
X1
= -0,7307 или 28,851 г/дм3 WO3;
X2
= 1 или 200 г/дм3 NaOH;
X3
= 1 или 70 оС.
Частные
зависимости удельной электропроводности растворов при значениях других
переменных на нулевом уровне приведены на рисунке.
Для
описания зависимости электропроводности щелочных растворов вольфрамата натрия
от температуры (25-70 оС) воспользовались формулой Кольрауша [4]:
ct = ct=25
[1 + a(t
– 25) + b(
t – 25)2], (4)
в
которой за стандартную температуру принята t=25 оС.
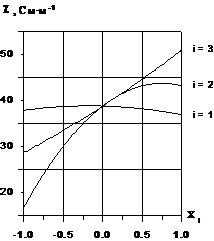
Частные
зависимости удельной электропроводности растворов.
Экспериментальные
данные хорошо описываются линейным уравнением вида
ct = ct=25
[1 + a(t
– 25)]. (5)
Расчетные
значения ct=25,
a,
а также коэффициента корреляции (rрасч) приведены в табл.3.
Т
а б л и ц а 3
Коэффициенты
математических моделей температурной зависимости удельной электропроводности
растворов и оценка адекватности
|
№
оп.
|
ct=25,
См/м
|
a,
град.-1
|
rрасч |
rкрит |
| 1,5 |
10,8376 |
0,016174 |
0,9998 |
0,6319 |
| 2,6 |
32,6967 |
0,020039 |
0,9999 |
0,6319 |
| 3,7 |
13,3439 |
0,018915 |
0,9997 |
0,6319 |
| 4 |
25,3974 |
0,026951 |
0,9993 |
0,6319 |
| 8 |
26,8049 |
0,018436 |
0,9998 |
0,6319 |
| 9 |
29,1996 |
0,023353 |
0,9995 |
0,6319 |
| 10,11 |
29,1448 |
0,016793 |
0,9999 |
0,6319 |
Чтобы
распространить полученные данные на растворы другого состава из изученной
области, получены модели зависимости удельной электропроводности растворов при
25 оС (ct=25)
и температурного коэффициента (a) от состава раствора (по WO3 и NaOH) в кодовом
масштабе:
ct=25 = 28,8810 – 1,2642 X1 + 8,4122
X2 – 0,5482 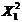 - 7,8299 - 7,8299 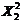 - -
- 2,4514 X1X2; (6)
Fрасч = 271,97; F0,05;6;1 = 234;
a =
0,01645 + 0,002328 X1 + 0,002952 X2 + 0,004045 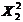 + +
+
0,001043 X1X2; (7)
Fрасч
= 105,90; F0,05;6;1 = 19,33.
Выполненные
исследования связаны с физико-химическим обоснованием процесса прямого
электрохимического растворения отходов металлического вольфрама в растворах
натриевой щелочи.
Список литературы
1.
Гуриев Р.А., Алкацев М.И. Электрохимическое растворение вольфрама под действием
переменного тока // Изв. вузов. Цв. металлургия. 1980. № 1. С. 61-64.
2.
Резниченко В.А., Палант А.А., Ануфриева Г.И., Гуриев Р.А., Гаврилов В.К.
Исследование процесса электрохимического растворения многофазных сплавов на
основе вольфрама // Изв. АН СССР. Мет. 1985. № 2. С. 32-35.
3.
Балихин В.С., Резниченко В.А., Корнеева С.Г., Корчагин И.В., Крепков П.Н. О
переработке отходов торированного вольфрама // Цв. мет. 1972. № 11. С. 65-67.
4.
Антропов Л.И. Теоретическая электрохимия. М.: Высшая школа, 1984. 519 с.
|