Контрольная работа: Защитные покрытия деталей РЭС-4
Контрольная работа: Защитные покрытия деталей РЭС-4
Введение
В производстве РЭС существует большое разнообразие покрытий как
целых устройств, так и элементов. Эти покрытия во многом определяют надежность
работы РЭС. Покрытия при производстве РЭС преследуют различные цели, среди которых
наиболее существенными являются: защита поверхности от коррозии; получение
красивого внешнего вида; придание поверхности изделия более высокой
механической прочности, высокой электропроводности.
По материалу пленок покрытия разделяются на металлические,
химические и лакокрасочные.
При выборе покрытия необходимо учитывать условия работы изделия и
отдельных деталей.
Легкие условия работы имеют герметизированные и теплоизолированные
детали, а также детали РЭС, устанавливаемые в закрытых помещениях, в которых не
содержатся промышленные газы.
Средние условия эксплуатации имеют детали негерметизированной
аппаратуры, работающей в условиях наружной атмосферы при Т – 60±70оС
и относительной влажности воздуха 70÷95%.
В жестких условиях работают детали негерметизированной РЭС при
непосредственном воздействии дождя и снега при температуре от -60÷+70оС
и относительной влажности воздуха до 98%, в условиях морской и тропической
атмосферы, а также РЭС, установленной в местах, доступных скоплению промышленных
газов.
1. Гальванические покрытия
Гальванические покрытия являются металлическими покрытиями и
широко используются для защиты поверхностей деталей от коррозии и придания им
красивого внешнего вида. Физической основой гальванических покрытий является
процесс электрохимического осаждения, то есть такое явление, при котором
постоянный электрический ток проходит через электролит и вызывает
электрохимическую реакцию разложения его. При этом на катоде происходит осаждение
чистого металла, а на аноде происходит реакция окисления и переход в электролит
положительно заряженных ионов металла анода. В качестве электролитов
используются растворы солей и кислот, тип и содержание которых определяется
видом гальванического покрытия.
В зависимости от характера защиты изделия от коррозии все
металлические покрытия подразделяют на анодные и катодные. Анодными называют
покрытия, электрохимический потенциал металла которых в данной среде более
электроотрицателен, чем электрохимический потенциал основания. Катодными
называют покрытия с обратным соотношением потенциалов. На рис. 1 показана
схема коррозии железа, покрытого цинковой (а) и медной (б) пленками.

Рис. 1. Схема коррозии железа, покрытого цинковой (а) и
медной (б) пленками
В случае нарушения целостности цинкового слоя и заполнения трещины
влагой образуется гальванический микроэлемент цинк-железо. Во внешней цепи
микроэлемента потечет ток от железного к цинковому слою, так как электродный
потенциал железа (-0,44 В) больше, чем у цинка (-0,76 В). Во внутренней цепи от
цинковой пленки к железному основанию катионы Zn2+ будут перемещаться
к аноду, а Н+ в направлении поверхности железа; пойдет реакция
вытеснения водорода по схеме
Zn2+ + H2O = ZnO + 2H.
Водород, выделившийся на поверхности железа в виде пузырьков газа,
защищает его от химической коррозии до тех пор, пока не растворится весь
цинковый слой. В этом случае цинковая пленка защищает основание от коррозии не
только механически, но и электрохимически.
В случае пленки из меди, ток в микроэлементе потечет во внешней цепи
от медного слоя (+0,34 В) к железу (-0,44 В). В этом случае катионы Fe3+
будут уходить в раствор, а Н+ к поверхности медной пленки. Реакция
вытеснения водорода пойдет по схеме
2Fe + 3H2O = Fe2O3 + 6H.
Следовательно, медная пленка не только не защищает основание от электрохимической
коррозии, но и поддерживает этот процесс. В случае катодного покрытия пленка
металла защищает основание механически, но не электрически.
В табл. 1 приведены значения электродных потенциалов чистых
металлов.
Таблица 1
| Металл |
Электродный потенциал |
Металл |
Электродный потенциал |
| Магний |
-2,4 |
Олово |
-0,14 |
| Алюминий |
-1,66 |
Свинец |
-0,126 |
| Цинк |
-0,76 |
Водород |
0,000 |
| Хром |
-0,71 |
Медь |
+0,34 |
| Железо |
-0,44 |
Палладий |
+0,799 |
| Кадмий |
-0,40 |
Платина |
+0,19 |
| Никель |
-0,23 |
Золото |
+0,42 |
При любом виде гальванических покрытий стремятся уменьшить
разность потенциала основного металла и покрытия с целью увеличения адгезии и
снижения электрохимической коррозии.
Основные требования, предъявляемые к гальваническим покрытиям:
высокая адгезия пленки, мелкозернистая структура, минимальная пористость, равномерная
толщина покрытия.
Технология нанесения гальванических покрытий состоит из
следующих основных этапов: подготовка поверхности; нанесение покрытия; промывка
и сушка; контроль толщины покрытия.
Подготовка поверхности заключается в механической обработке,
обезжиривании и травлении.
Механическую обработку производят с целью повышения чистоты
поверхности, удаления неровностей (заусенцев, острых кромок, сварочных брызг),
продуктов коррозии. Для этих целей в гальванических цехах применяют
гидропескоструйную обработку, шлифование и полирование, галтовку (обработку во
вращающихся барабанах с загруженными опилками, песком и т.д.), крацевание
(обработку стальными, медными или латунными щетками).
Для удаления жировых загрязнений животного и растительного
происхождения применяют химическое обезжиривание в водных растворах: едкого
калия (КОН) или едкого натра (NaOH), кальцинированной соды (NaCO3),
жидкого стекла (NaSiO3). Удаление загрязнений
минерального происхождения (минеральных смазок, масел) производят предварительной
промывкой деталей в органических растворителях (бензин, керосин), с последующей
обработкой более энергичными растворителями – ацетоном (С3H6O),
трихлорэтиленом (С2HСl4), четыреххлористым углеродом (ССl4).
Хороший эффект удаления жировых загрязнений, особенно с
поверхностей мелких деталей, получают при ультразвуковой очистке, которую
осуществляют в специальных ваннах с водными растворами щелочей или с
органическими растворителями. Кроме того, ультразвуковая очистка применяется
для удаления полировочных паст после полирования.
Травление применяется для удаления с поверхности пленок и окислов
обезжиренных и промытых деталей. Травление производится обычно в растворах
серной, соляной и азотной кислоты. Заключительной операцией подготовки
поверхности является декапирование (легкое травление), которое осуществляется
погружением деталей в 5–10 процентный водный раствор серной или соляной кислоты,
или их смеси.
Для гальванических покрытий мелких деталей применяют вращающиеся
ванны (колокола) с наклонной осью вращения. Колокол, изготовленный из стали,
внутри покрыт резиной или термопластичной пластмассой, на которые укладывают
медные контактные пластины – катоды. Анодная пластина крепится на неподвижно
крепящейся штанге. Детали насыпают на дно ванны, наполненной соответствующим
электролитом. Во время покрытия колокол вращается, что обеспечивает равномерное
осаждение металла по поверхностям всех деталей. Крупные детали покрываются в
стационарных ваннах, которые оборудуются специальными транспортерами,
обеспечивающими перемещение деталей параллельно анодам.
После нанесения покрытий деталей осуществляется их промывка
сначала в горячей проточной воде, а затем в проточной холодной воде с
последующей сушкой в струе сжатого воздуха.
Процесс гальванических покрытий производят на автоматизированных
линиях, выполняющих основные операции: перемещение деталей из одних ванн в
другие, подача растворов, регулирование режимов температуры, плотности тока.
Контроль качества покрытий заключается в определении прочности
сцепления пленок с поверхностью материала детали и толщины пленки.
Различают качественные и количественные методы определения
прочности сцепления.
К качественным относятся методы: полирования, нагрева до
определенной температуры, многократного изгиба под углом 90о. При этом
не должно наблюдаться вздутий или отслаивания пленки.
Количественный метод контроля основан на определении силы,
необходимой для отрыва пленки от металла детали.
Контроль толщины покрытия осуществляют химическими и физическими
неразрушающими методами.
К химическим методам относится, например, метод капли, сущность
которого заключается в следующем. На гальваническую пленку при помощи
капельницы наносят каплю растворителя, состав которого зависит от типа
покрытия, и выдерживают одну минуту. После поверхность насухо протирают и затем
наносят вторую каплю и так до тех пор, пока не обнаружится поверхность металла
детали. Толщину слоя в мкм (δ) определяют из соотношения δ = (N – 1) K (N – число капель, K – толщина слоя,
растворяемого за 1 мин). Однако этот метод в настоящее время мало
применяется из-за его трудоемкости.
Более совершенными и высокопроизводительными являются физические
(неразрушающие) методы: магнитный и электромагнитный, позволяющие определять толщину
немагнитных пленок, нанесенных на магнитные металлы; метод вихревых токов,
который позволяет измерять толщину немагнитных и слабомагнитных пленок,
нанесенных на немагнитные металлы.
В производстве радиоэлектронных средств применяются следующие
гальванические покрытия.
Цинковое покрытие применяется для защиты от коррозии стали
и чугуна; по стали оно является анодным. Цинковое покрытие имеет среднюю
твердость, выдерживает изгибы, развальцовку, хорошо паяется мягкими припоями,
сваривается. Во влажной среде на поверхности образуется окисная пленка. При температуре
+ 80оС цинк быстро корродирует, морская вода разрушает его. Для
цинкования применяются кислые (на основе солей ZnSO4, Na2SO4) и щелочно-цианистые (ZnO, NaCN, NaOH) электролиты. Вторые
позволяют получить более качественные покрытия и их применяют при покрытии
сложных деталей, однако они сильно ядовиты. Процесс цинкования ведут при плотностях
тока 100–200 А/м2.
В настоящее время в РЭС для защиты от коррозии белые цинковые
покрытия не применяются вследствие их малой стойкости. Для этого на последней
операции цинкования детали подвергаются хроматированию в солях двухромового
натрия. Для хроматирования детали с цинковым покрытием промывают в проточной
воде, а затем переносят в хроматную ванну, где выдерживают в течение нескольких
секунд. В результате этого получается цинковое радужное покрытие, более стойкое
против действия агрессивных сред.
Цинковое покрытие применяется для защиты деталей, работающих в
легких и средних условиях эксплуатации. Толщина покрытия составляет 6 – 30 мкм.
На чертежах цинковое покрытие обозначается Ц.9.хр (цифра 9 обозначает толщину
покрытия в мкм, хр – хроматирование).
Медное покрытие применяется как подслой при нанесении никеля,
хрома, серебра и других металлов (медные покрытия не обладают надежными
антикоррозионными свойствами), а также в технологических целях для защиты
отдельных поверхностей стальных деталей от цементации, при изготовлении проводников
печатных плат. Толщина пленок составляет 3 – 25 мкм. Для меднения применяются
кислые (CuSO4, H2SO4) или цианистые (CuCN, NaCN, NaCO3) электролиты. Медные покрытия обозначаются – М.6 (цифра 6
обозначает толщину слоя в мкм).
Кадмиевое покрытие применяется для защиты от
коррозии стали, чугуна, меди и медных сплавов, алюминия и его сплавов – в этом
случае применяют многослойное покрытие. Кадмий обладает более высокой
коррозийной стойкостью, чем цинк. Более стоек к действию минеральных кислот,
совершенно не растворим в щелочах. Кадмиевое покрытие не разрушается при гибке,
вытяжке, развальцовке, хорошо паяется. Под действием влажной атмосферы
кадмиевое покрытие покрывается тонкой пленкой окиси. Если в атмосфере
присутствуют сернистые соединения, то кадмиевая пленка быстро разрушается. Поэтому
для увеличения стойкости против действия внешней среды кадмиевые покрытия
подвергаются хроматированию. После хроматирования кадмиевые покрытия
приобретают радужный оттенок.
Кадмиевое покрытие применяют для защиты от внешних воздействий при
средних (толщина слоя 9 – 15 мкм) и жестких (толщина слоя 15 – 30 мкм) условиях
эксплуатации радиоэлектронных средств. На чертежах кадмиевое покрытие обозначают
Кд.15. хр, а при многослойном покрытии деталей из алюминиевых сплавов – Н9.М6. Кд9
хр (Н – слой никеля, М – слой меди).
Для кадмирования используют кислые и цианистые электролиты.
Последние обладают высокой рассеивающей способностью и образуют плотный
мелкокристаллический слой, поэтому их применяют для покрытия сложных и
ответственных деталей. Ограничением по применению кадмиевых покрытий является более
высокая стоимость по сравнению с цинковым покрытием и высокая токсичность
кадмия и его соединений.
Никелевое покрытие широко применяется как защитно-декоративное
покрытие деталей РЭС из сталей и алюминиевых сплавов, работающих в легких и
средних условиях эксплуатации. Это покрытие имеет высокую механическую
прочность, коррозионную стойкость и красивый внешний вид. Однако никелевое
покрытие по стали и алюминиевым сплавам является катодным, а следовательно, не
защищает их электрохимически и вместе с тем оно отличается пористостью. Поэтому
никелирование стальных и алюминиевых покрытий производят с подслоем меди; толщина
слоя никеля обычно составляет 3–9 мкм. Никелевые покрытия также являются
основой многослойных систем Ni-Cr и Cu-Ni-Cr.
Операция никелирования выполняется в электролитах, главной
составной частью которых являются сернокислый никель, хлористый калий и борная
кислота (NiSO4, KCl, H3BO3). Условное
обозначение никелевых покрытий в конструкторской документации имеет вид: М6.Н3
– для деталей из стали; Н9.М6.Н9 – для деталей из алюминиевых сплавов.
Хромовое покрытие используется для защиты от коррозии деталей из стали,
меди, алюминия и никеля, а также для повышения отражательной способности
поверхности (до 70%), износоустойчивости, жаростойкости и твердости. Хром отличается
высокой коррозийной стойкостью во влажной среде, щелочных, азотной и
органических кислотах, в атмосфере большинства газов, не тускнеет при
нагревании до 500оС. Недостатком хромовых покрытий является плохое
смачивание маслами и припоем, высокая пористость и неравномерное распределение
по поверхности. Применяют два вида хромирования: защитно-декоративное и
функциональное для увеличения твердости и износостойкости поверхности (инструментов,
штампов и др.). Толщина слоя хрома в первом случае составляет 1–2 мкм и
хромирование производят с подслоем никеля. При функциональном назначении
покрытия толщина слоя хрома находится в пределах 10–60 мкм, а хромирование
осуществляют без подслоя. В качестве электролита при хромировании применяют
растворы на основе хромового ангидрида (CrO3) и серной кислоты (H2SO4). Аноды изготавливают из сплава свинца (92%) и сурьмы (8%).
Поэтому при хромировании необходимо следить за содержанием хромового ангидрида
в электролите и своевременно добавлять его в электролит. Процесс хромирования
производят при температуре 50 оС и плотности тока около 2500 А/м2
(для защитно-декоративного покрытия) Т = 60оС и плотности тока
4500 А/м2 (для функционального покрытия). В процессе хромирования
происходит насыщение пленок хрома водородом, что придает ему хрупкость. Для устранения
водородной хрупкости детали после хромирования тщательно промывают и затем
подвергают термообработке при температуре 150–200оС в масле.
Необходимость использования высокой температуры и большой
плотности тока при хромировании требует применения эффективной вытяжной
вентиляции, так как выделяющиеся пары хромовых соединений очень вредны для
человека.
В конструкторских и технологических документах хромовые покрытия
имеют следующие обозначения: М6.Н3.Х1 – защитное покрытие по стали; Н6.Х1 – защитное
покрытие по меди; Н9.М6.Н9.Х1г – защитно-декоративное покрытие алюминия (г –
глянцевое); Х.48 – покрытие стали для увеличения твердости и защиты от
коррозии.
Оловянно-свинцовое покрытие применяется для защиты деталей из
стали, меди и ее сплавов от коррозии и подготовки поверхности к пайке. Луженые
поверхности хорошо противостоят воздействию многих органических кислот и
воздействию паров серы. Толщина покрытия жил медного провода составляет 4–6
мкм, для подготовки поверхности к пайке – 10–20 мкм.
В качестве анода применяется припой ПОС-61. В электролит входит
борфтористоводородная кислота (HBF4), ее оловянные и свинцовые соли
и борная кислота H3BO3. Для уменьшения образования
крупных кристаллов (дендритов), имеющих слабую адгезию к основанию, в раствор
вводят фенол. Гальванический слой через 10 суток хранения быстро окисляется,
что затрудняет пайку. Кроме того, при хранении может наблюдаться появление
игольчатых наростов "усов", которые в микроэлектронике могут вызвать
короткое замыкание. Поэтому после гальванического осаждения поверхность
оплавляют, что устраняет эти нежелательные эффекты.
Оловянно-свинцовое покрытие обозначают: ПОС-61.9 – покрытие по меди
и ее сплавам (цифра 9 – толщина слоя); М18 ПОС-61.9 – покрытие по стали.
Серебряное покрытие применяется в основном для улучшения
электропроводности поверхности детали: высокочастотных разъемов; деталей,
работающих в СВЧ диапазоне, и др. Оно отличается высокой электропроводностью и
отражающей способностью, коррозионной стойкостью против щелочей и некоторых
органических кислот (растворяется в азотной кислоте).
Недостатком серебряных покрытий является невысокая механическая
прочность, и на него сильно действуют сернистые соединения (серебро тускнеет и
чернеет). Серебрению подвергают изделия из черных и цветных металлов, причем детали
из стали предварительно покрывают медью. Серебрение производится в
электролитах, содержащих цианистые электролиты (на основе хлористого серебра и
цианистого калия) и безцианистые электролиты (на основе хлористого серебра,
углекислого калия и железисто-синеродистого калия). При серебрении в цианистых
электролитах необходимо соблюдать особые меры предосторожности из-за высокой
токсичности этих соединений.
Для увеличения механической прочности серебряных покрытий,
например контактных пар штепсельных разъемов, электрических контактов и др., их
покрывают пленкой родия или палладия, имеющих большую твердость, химическую
стойкость и стойкость против электрической эрозии.
Для защиты от действия сернистых соединений серебряные покрытия
подвергают хромированию в растворе двухромового натрия (Na2CH4O7).
Серебряные покрытия имеют следующие обозначения: Ср.9 хр –
покрытие по меди и ее сплавам; Н9.М6. Ср9 – многослойные покрытия по алюминию и
его сплавам; Ср6. Пд3 – покрытие по меди и ее сплавам с пленкой палладия; Ср9. Рд1
– покрытие меди и ее сплавов с пленкой родия.
Золотое покрытие применяют для защиты: от внешних воздействий,
повышения износостойкости и увеличения электропроводности деталей наиболее
ответственного назначения, деталей высокочастотных и СВЧ трактов; электрических
контактных пар; электрических выводов интегральных схем и др. Золото является
наиболее коррозионно-стойким металлом, оно не подвержено действию кислот,
щелочей, сероводорода и других соединений серы, обладает высокой прочностью и
электропроводностью (по электропроводности оно уступает только серебру и меди).
Только немногие химические соединения растворяют золото. К ним принадлежит
смесь из трех объемных частей соляной кислоты и одной – азотной кислоты ("царская
водка"), а также цианидные растворы, агрессивные в присутствии кислорода.
В зависимости от назначения деталей толщина золотого покрытия
колеблется в пределах 1–5 мкм. Для повышения твердости поверхности золото
осаждают вместе с никелем (твердое золочение). При золочении стальных деталей
их предварительно меднят.
В качестве электролитов при золочении применяют цианистые (на
основе комплексной цианистой соли золота и цианистого калия) и бесцианистые (на
основе золотохлористой водородной кислоты и железистосинеродного калия)
электролиты. При золочении необходимы особые меры предосторожности, так как
цианистые электролиты сильно ядовиты.
Золотые покрытия имеют следующие обозначения: З.1 – покрытие по
меди и ее сплавам; М35.З1 – покрытие по стали и сплавам на основе железа.
2. Химические покрытия
Химические покрытия представляют собой тонкий слой защитной
пленки, образующийся на поверхности детали за счет
окислительно-восстановительных процессов, протекающих в процессе получения
защитного покрытия. Различают два вида химических покрытий: оксидные и
фосфатные, которые образуются в результате химического взаимодействия
определенных химических растворов с металлами детали; химические пленки
металлов, получаемые в результате восстановительных процессов в растворах,
содержащих соли металла.
Химические пленочные покрытия служат для повышения стойкости
материала деталей к коррозии, износостойкости, электропроводности и т.п.
Основные требования, предъявляемые к этим покрытиям: прочное сцепление с
покрываемой поверхностью, отсутствие пористости. Равномерность толщины слоя по
всей поверхности.
Перед нанесением химических покрытий детали подвергают
механической обработке, обезжириванию и травлению для удаления окисной пленки и
выявления структуры основного металла.
В производстве РЭС наибольшее применение получили оксидные и
фосфатные покрытия на деталях, изготовленных из алюминиевых, магнитных сплавов
и сплавов на основе железа.
Оксидные покрытия на алюминиевых сплавах обладают высокой
коррозионной стойкостью и твердостью, повышенной теплостойкостью и электроизоляционными
свойствами. На поверхности алюминия всегда образуется естественная оксидная
пленка толщиной около 0,1 мкм, но она не гарантирует защиту деталей в средних и
тяжелых условиях эксплуатации.
Более стойкие оксидные покрытия получают химическим оксидированием
и электрохимическим оксидированием, получившим название анодирования.
Химическое оксидирование применяют для деталей сложной формы.
Процесс состоит в погружении деталей в ванну с раствором на основе соды
кальцинированной (NaCO3), хромовокислого натрия (Na2Cr2O7) и воды, время выдержки 3–5 мкм. Толщина окисных пленок при этом составляет
2 – 5 мкм. Для лучшей защиты от действия внешней среды окисные пленки
обрабатывают (хроматируют) в 2%-ном растворе окиси хрома (СrО3),
который заполняет поры и нейтрализует щелочи в порах. Химическое оксидирование
является дешевым и простым способом защиты деталей.
Следует отметить, что на швах, полученных в результате пайки
оловом, оловянисто-свинцовым или серебряным припоем, оксидное покрытие не образуется.
Электрохимическое оксидирование (анодирование) выполняют в
электролите постоянным или переменным током. При анодировании постоянным током
детали завешивают на анод, а катодом служат свинцовые пластины, а при
анодировании переменным током детали завешивают на оба электрода.
В качестве электролитов применяют водные растворы серной,
щавелевой или хромовой кислоты. Для обеспечения большей надежности детали
бортовой аппаратуры анодирование выполняют в растворах щавелевой и хромовой
кислоты. Толщина анодных покрытий составляет 10–100 мкм, при этом размер
деталей не изменяется, так как процесс образования пленки происходит за счет
металла детали. Окисная пленка состоит из внутренней плотной тонкой пленки и
внешней пористой пленки, поэтому анодные окисные пленки могут пропитываться для
получения различных свойств поверхностей деталей. При пропитке водным раствором
черного анилинового красителя получаются матово-черные поверхности с малым отблеском.
Жаростойкие пленки могут быть получены пропиткой светочувствительными солями
серебра. Толстые пленки, пропитанные маслом, применяются для направляющих
полозьев выдвижных блоков, твердость такой пленки близка к твердости закаленной
стали.
Толстые окисные пленки, полученные электрохимическим способом,
применяются не только как защитные, но и как диэлектрические. Диэлектрические
пленки на алюминиевой фольге, тантале применяются для изготовления
электрических конденсаторов.
Оксидные покрытия имеют следующие обозначения: Хим. Окс –
химическое окисное покрытие; Хим. Окс.хр – химическое окисное с
хроматированием; Ан. Окс.10.хр – анодизационное окисное (толщина 10 мкм) с
хроматированием.
Оксидные покрытия на магниевых сплавах применяют для защиты от
коррозии поверхности деталей. Магний относится к активным элементам, его
электродный потенциал составляет -2,4 В. Магниевые сплавы находят применение
для изготовления деталей бортовой радиоэлектронной аппаратуры, так как они
обладают малым удельным весом и высокой удельной жесткостью, и удельной прочностью.
Оксидные покрытия получают методами химического оксидирования и
электрохимического оксидирования (анодирования).
Операция оксидирования состоит в погружении деталей в водный
раствор, состоящий из хромовокислого калия (К2Cr2O7), азотной кислоты (НNO3) и хлористого
аммония (NH4Cl). Время выдержки в растворе составляет 2–3 мин, а толщина
защитной пленки 6–8 мкм. После оксидирования детали должны тщательно промывать
в холодной, а затем в горячей воде.
Электрохимическое оксидирование (анодирование) применяют для получения
более толстых защитных пленок (до 10–15 мкм). Анодирование производят в водном
растворе хромовокислого калия (K2Cr2O7) тринатрийфосфата (Na3PO4). Детали навешиваются на
анодную шину, а катодом служит железная пластина. Обозначение покрытий подобно
обозначению на деталях из алюминиевых сплавов.
Оксидные покрытия по стали состоят из окисных соединений железа
(FeO, Fe2O3, Fe3O4). Защитные свойства пленки зависят от ее толщины и режима
оксидирования. Бывают три способа оксидирования – термический, химический и
электрохимический.
Термический способ (воронение) заключается в нанесении на деталь
тонкого слоя асфальтового или масляного лака, сушке на воздухе и термической
обработке при температуре около 350оС с последующим охлаждением в
минеральном масле. Обработанные таким образом детали имеют защитную пленку из
окислов железа, покрытого тонким слоем асфальта или осмоленного лака.
При химическом способе воронения детали погружаются в
расплавленные соли, например, смеси селитры и двуокиси марганца, нагретые до
температуры 350оС. При этом на поверхности появляется защитная
пленка черного цвета. Для получения пленки синего цвета детали погружаются в
раствор солей, состоящий из нитрата натрия и нитрита натрия, и выдерживают при
температуре около 310оС.
Фосфатные покрытия имеют лучшие защитные свойства, чем
оксидные, не разрушаются и не теряют своих свойств, при кратковременном нагреве
до температуры 400оС, обладают высоким электрическим сопротивлением и
высокой электрической прочностью (выдерживают электрическое напряжение от 250
до 1200 В). Фосфатные пленки имеют пористую и губчатую структуру, поэтому
хорошо удерживают смазки и обладают высокой прочностью сцепления с
лакокрасочными покрытиями. Фосфатные пленки применяют как изоляционное покрытие
пластин магнитопроводов, трансформаторов и различных деталей, работающих в
легких, средних и жестких условиях эксплуатации.
Фосфатирование стальных деталей производится в растворе МАЖЕФ, содержащем
марганцевые и железистые фосфаты. Фосфатирование ведется при температуре 80–90оС
в течение 5–10 мин.
Фосфатирование деталей из алюминия и его сплавов осуществляется
кипячением в 10%-ном растворе ортофосфорной кислоты с добавлением бихромата
калия и фториевого натрия.
Кроме химических фосфатных покрытий бывают окисно-фосфатные
покрытия, которые применяются для защиты от коррозии сплавов на основе алюминия
при средних и тяжелых условиях эксплуатации. Окисно-фосфатные покрытия
производят в растворе фосфорной кислоты, азотнокислого кальция и перекиси
марганца. При этом покрытия получаются красивого черного цвета. Фосфатные
покрытия имеют следующие обозначения: 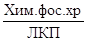 –
химическое фосфатное с хроматированием, с последующим лакокрасочным покрытием;
Хим. Окс. Фос. – окисно-фосфатное покрытие. –
химическое фосфатное с хроматированием, с последующим лакокрасочным покрытием;
Хим. Окс. Фос. – окисно-фосфатное покрытие.
Химические металлические покрытия применяют для защиты от
коррозии, повышения электропроводности, износостойкости, декоративной отделки
деталей из металлов и пластмасс. Металлические покрытия получают методом химической
металлизации в специальных растворах. Химическая металлизация основана на
протекании в растворах окислительно-восстановительных реакций, при которых
происходит восстановление ионов осаждаемого металла на поверхности детали.
Химическое меднение поверхностей стальных деталей выполняют
погружением их в водный раствор, состоящий из сернокислой меди и серной
кислоты.
Химическое серебрение применяют для повышения электропроводности и
отражательной способности деталей из меди и ее сплавов. Серебрение осуществляют
в цианистых электролитах.
Химические никелевые покрытия содержат до 15% фосфора и обладают
высокой коррозионной стойкостью, твердостью и износостойкостью. Никелевые
покрытия применяют для защиты от коррозии корпусов гибридных интегральных схем,
увеличения износостойкости штепсельных разъемов из бронз и др. Химическое
никелирование ведут в растворах, содержащих щелочные или кислые растворы солей
никеля и гипофосфита.
Химическое лужение (оловянирование) применяют для защиты деталей
от коррозии, подготовки поверхности под пайку, герметизации плотных сопряжений
деталей в сборочных единицах и т.д. Химическое лужение деталей из алюминиевых
сплавов проводят в растворе на основе хлорного олова и едкого натра при
температуре 70–75оС.
Лужение стальных деталей осуществляют в кипящем растворе хлорного
олова, насыщенного однозамещенным виннокислым калием (КС4Н5О6).
Химические покрытия деталей из пластмасс используют как
электропроводящие и отражательные слои на поверхности диэлектриков.
Химическое меднение пластмассовых деталей состоит из операций
подготовки поверхности (например, крацеванием или обдувкой поверхности песком),
сенсибилизации и меднения. Сенсибилизация – это процесс нанесения на
поверхность диэлектрика очень тонкой пленки металла, способствующего последующему
осаждению меди из химических растворов. Для сенсибилизации применяют водные
растворы азотнокислого серебра или раствор двухлористого олова.
При создании проводников печатных плат химическим способом перед
меднением проводят сенсибилизацию в растворе двухлористого олова и активацию
поверхности в растворах солей благородных металлов, преимущественно палладия.
Для улучшения качества металлизации часто применяют совмещенный раствор для
сенсибилизации и активации (совмещенный активатор) на основе двухлористого
палладия и двухлористого олова с добавлением соляной кислоты и хлористого
калия. Наращивание слоя меди осуществляют в химических растворах, содержащих
соли меди, например в растворе сернокислой меди с добавлением едкого натрия,
виннокислого калий-натрия (КNaC4H4O6) и углекислого натрия.
Процессы химического серебрения диэлектриков состоят из
сенсибилизации поверхности с последующим осаждением серебра из растворов. В
качестве сенсибилизаторов чаще всего применяют водный раствор хлористого олова.
Химическое восстановление серебра осуществляют в растворах, содержащих
азотнокислое серебро, едкий натр, аммиак. Применяют и другие химические
растворы для химического наращивания серебра. Серебряные пленки используют для
создания проводящих и зеркальных поверхностей на диэлектриках.
3. Покрытия, полученные методом электрофореза
Пленки, полученные методом электрофореза, обладают высокой
адгезией к поверхности металлических изделий, плотностью, прочностью и высокими
электроизоляционными свойствами.
Сущность электрофорезного способа состоит в том, что при наличии
разности потенциалов в суспензионном растворе, в котором частицы порошка
находятся во взвешенном состоянии (коллоидные частицы), происходит движение
последних к электроду и осаждение их на поверхности. Таким образом, происходит
осаждение неметаллического материала на поверхности металлического изделия,
которое является анодом. После электрофореза изделие подвергают сушке и
термообработке. При термообработке происходит спекание частиц и образуется
твердое и гибкое покрытие с высокими электроизоляционными свойствами. Толщина
слоя покрытия регулируется плотностью тока, напряжением и временем выдержки изделия
в растворе.
В качестве коллоидных растворов при электрофорезе применяют
следующие составы:
суспензионный раствор кремниевой кислоты в ацетоне;
суспензионный раствор окиси магния в четыреххлористом углероде;
раствор каолина в воде.
Метод электрофореза широко применяется для нанесения межслойной
изоляции магнитопроводов, изготавливаемых из лент методом навивки. Наиболее
широкое применение в этом случае получил суспензионный раствор кремниевой
кислоты в ацетоне.
На рис. 2 изображена схема технологической установки для
нанесения изоляции лент из электротехнической стали или железоникелевых сплавов
методом электрофореза.
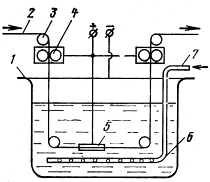
Рис. 2
В ванну 1 с коллоидным раствором кремниевой кислоты в ацетоне
подается обезжиренная лента 2 с помощью роликов 3 и 4. На ванну подается
отрицательный потенциал, а на ленту положительный потенциал. Для лучшего
осаждения коллоидных частиц раствор постоянно перемешивается сжатым воздухом
через отверстия в трубе 6. В результате электрофореза на поверхности ленты
осаждаются частицы, состоящие из окиси кремния SiO2. Толщина
изоляционного слоя обычно составляет 5–10 мкм. Электрофоретическая ванна
встраивается в автоматическую линию при изготовлении ленточных магнитопроводов
методом навивки.
Процессы электрофореза применяют для нанесения пластмасс на
металлы; в этом случае слой из пластмассы является защитным от действия внешней
среды.
4. Лакокрасочные покрытия
Лакокрасочные покрытия представляют собой неметаллические пленки,
применяемые для защиты поверхности деталей от воздействия внешней среды и
придания им красивого внешнего вида. Их нельзя применять для деталей, имеющих
точные размеры и трущиеся поверхности, подвергающиеся механическим воздействиям
и нагреву. Основными требованиями к лакокрасочным покрытиям являются:
непроницаемость пленок для газов и жидкостей; хорошая адгезия к поверхности металлических
и неметаллических изделий; высокая термостойкость в заданном интервале
температур и высокие электроизоляционные свойства. Для аппаратуры, работающей в
тропических условиях, добавляются требования по стойкости против грибковой
плесени, грызунов и термитов.
Основными компонентами лакокрасочных покрытий являются
пленкообразующие вещества, наполнители, пигменты, пластификаторы и
растворители.
Основой лакокрасочных покрытий являются пленкообразующие вещества,
к которым относятся растительные масла (льняное, тунговое), битумы, природные и
синтетические смолы (шеллак, канифоль, феноло-и креозолоформальдегидные, эпоксидные,
кремнеорганические, алкидные, полиэфирные). При высыхании они образуют прочную
пленку.
Пигменты – высокодисперсные неорганические вещества (железный
сурик, диоксид титана, охра и др.), создающие цветовой оттенок и повышающие
твердость и механическую прочность лакокрасочных покрытий.
Наполнители – неорганические и органические порошкообразные
материалы (пылевидный кварц, тальк, графит, слюдяная пыль и др.), повышающие
влагостойкость, уменьшающие температурный коэффициент линейного расширения и
улучшающие антикоррозионные свойства покрытий.
Пластификаторы применяют для повышения эластичности и ударной
прочности защитной пленки. В качестве пластификаторов используют нелетучие
вещества – дибутилфталат, трибутилфосфат, нефтяные масла, касторовое и льняное
масло.
Растворители – летучие органические жидкости, применяемые для
растворения красок и лаков и улетучивающиеся в процессе образования пленки и
способствующие получению равномерной толщины защитного покрытия. Растворителями
служат ароматические углеводороды, спирты, сложные и простые эфиры, скипидар и
др.
В состав лаков и красок могут входить следующие дополнительные
вещества: отвердители и сиккативы.
Отвердители – это вещества (кислоты, соли, изоцианы и др.),
которые способствуют образованию пленок на основе реакционноспособных
олигомеров, например на основе эпоксидных смол. Сиккативы вводятся для
ускорения процесса высыхания лакокрасочных материалов, содержащих растительные
масла. В качестве сиккативов используют растворимые в маслах соли некоторых
металлов (кобальта, марганца, кадмия, цинка и др.).
Защитные свойства лакокрасочных покрытий определяются свойствами
пленкообразователя, пигмента и технологией нанесения покрытия.
Технология нанесения лакокрасочных покрытий состоит из следующих
основных этапов: подготовки поверхности, окраски и сушки.
Подготовка поверхности включает в себя очистку поверхности,
грунтовку и шпатлевание.
Очистку поверхности осуществляют механическим (галтовка,
крацевание, гидропескоструйная обработка или шлифование) или химическим
(обезжиривание, травление) способами.
Грунтовка состоит в нанесении на поверхность детали слоя грунта.
Цель грунтовки – улучшение адгезии лакокрасочного покрытия с поверхностью
детали и придание дополнительной защиты от действия внешней среды. Для
грунтовки применяют лакомасляные, битумномасляные, нитро- и водоразбавляемые
грунты. Во многих случаях для повышения коррозионной стойкости изделий,
работающих в жестких или особо жестких условиях, поверхности предварительно
фосфатируют или оксидируют. Грунт наносят распылением, окунанием или кистью.
После нанесения слоя грунта производят сушку.
Шпатлевание – выравнивание загрунтованной поверхности. Шпатлевание
применяют в тех случаях, когда к поверхности предъявляют повышенные требования
по внешнему виду, а поверхность имеет дефекты. Шпатлевка представляет собой
пастообразную массу, состоящую из пигментов, наполнителей и лаков с добавлением
или без добавления пластификаторов. Применяют лаковые, масляные, клеевые,
нитроцеллюлозные, перхлорвиниловые и эпоксидные шпатлевки. Шпатлевки наносят на
поверхность при помощи шпателя или краскораспылителя – в этом случае их
разбавляют растворителем. Зашпатлеванные детали сушат и шлифуют
механизированным инструментом.
Окраску деталей производят с помощью кисти, окунанием и
распылением. Окрашивание кистью является малопроизводительным методом, который применяют
для медленно сохнущих лаков, покраски поверхности и нанесения обозначений по
трафарету. Нанесение лакокрасочных покрытий окунанием применяют для деталей, не
требующих тщательной отделки и имеющих форму, удобную для стекания краски. В
этом случае получается неравномерное по толщине покрытие и большой расход
материала. Окрашивание распылением является более высокопроизводительным
процессом, при этом получается высокое качество поверхности, но этот способ
связан с повышенным расходом материала и окрашивание необходимо вести в
специальной камере.
Наиболее совершенным способом является окраска в электростатическом
поле (рис. 3). При этом способе изделия подвешиваются на заземленный
конвейер 4, проходящий между электродами 1, на которые подается отрицательный
потенциал от источника напряжения 2. Краску подают воздушными распылителями 3
на движущиеся изделия, находящиеся в электрическом поле. Частицы краски,
заряжаясь отрицательно, притягиваются к положительно заряженным деталям.
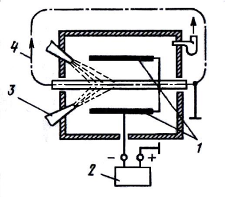
Рис. 3
При этом способе повышается производительность труда (в 3–4 раза),
улучшаются санитарные условия труда, повышается качество покрытия (разброс по толщине
составляет 5–8 мкм), сокращается расход лакокрасочных материалов (потери
составляют всего 5–10%) и создаются условия комплексной автоматизации процесса
окраски.
Сушка является заключительным этапом. При выборе способа и режима
учитывают многие факторы: вид лакокрасочного материала, характер покрываемой
поверхности деталей, их размеры и конфигурация, поточность производства и др.
Сушка может быть при обычной температуре окружающего воздуха (естественная
сушка) и принудительная при повышенных температурах (в сушильных шкафах,
рефлекторных сушилках и т.д.). Наиболее совершенна сушка инфракрасными лучами.
|