Дипломная работа: Оценка качества очистки сточных вод
Дипломная работа: Оценка качества очистки сточных вод
Оценка качества очистки сточных вод
Дипломная работа
Выполнил студент 5 курса Астепкин Р.Е.
Челябинск - 2006 г
Введение
Вода - самое
распространенное неорганическое соединение на нашей планете. Это ценнейший
природный ресурс. Она играет исключительно важную роль в процессах обмена
веществ, составляющих основу жизни. Огромное значение вода имеет в промышленном
и сельскохозяйственном производствах. Общеизвестна необходимость ее для бытовых
потребностей. Вода входит в состав организма человека, всех растений и
животных. Для многих живых существ она служит средой обитания.
Вода – непременный агент
фотосинтеза. Она имеет высокую диэлектрическую проницаемость, благодаря чему
присоединяет и удерживает почти все вещества. Это отличительный теплоноситель и
охладитель. Вода обладает таким уникальным качеством, как большое поверхностное
натяжение, вследствие чего способна подниматься по капиллярам в почве.
Совершая круговорот в
природе, вода участвует в формировании поверхности Земли. Она разрушает, растворяет
и транспортирует неорганические вещества, способствует отложению осадочных
пород и образованию почвы.
Вода оказывает
существенное влияние на климат и погоду, так как обладает высокой теплоемкостью
и низкой теплопроводностью. Аккумулируя солнечное тепло, она при больших
скоплениях выравнивает годичные и суточные колебания температуры.
В мире на одного человека
ежегодно расходуется в среднем 30 м3 воды, из них 1 м3 для питья. В некоторых странах на одного человека приходится всего 2 м3 воды в год. Здесь она оказывается одним из самых дорогих ресурсов. В нашей стране в мелких
населенных пунктах потребление воды не превышает 30 л в сутки на 1 человека, в некоторых районах – даже 5-6 л. В жилищах с канализацией и водопроводом
оно достигает 200 л/сут, а в домах, оборудованных горячим водоснабжением, - еще
выше.
Водная среда, водоемы в
зависимости от санитарного состояния могут быть местами развития организмов, которые
по-разному приспособлены к уровню загрязнения и процессам, происходящим в этих
условиях.
Речная вода более или
менее постоянного состава, однако, во время весенних паводков, ливневых дождей
в результате большого стока вода делается мутной, в ней нередко появляются
химические вещества, используемые для удобрения. Качество зависит от сезона
года, а так же местности, в которой протекают реки.
Соленые воды составляют
94, 2 % всех водных ресурсов Земли. Они занимают свыше 70% поверхности земного
шара, но используются недостаточно. Запасы же пресной воды на Земле
незначительны: с учетом части подземных вод их около 30 млн км3. Причем большая
часть этой воды (97%) приходится не ледники Антарктиды, Гренландии, полярных
островов и гор. Если бы весь лед распределить равномерно по поверхности Земли, то
образовался бы слой толщиной 53 м.
Цель работы – оценить
качество очистки сточных вод МУП «Водоканал» г. Тотьма.
Задачи:
Исследовать качественный
и количественный состав сточных вод, поступающих на очистку, и сбрасываемых в
водоем.
Определить качественные
показатели реки Сухона в связи со спуском в нее сточных вод г. Тотьма.
§ 1. Литературные сведения
Санитарно – гигиеническое
значение воды
Вода является основным
компонентом любой живой ткани. Вода в организме находится в трех жидкостных
фазах: внутриклеточной, внеклеточной, трансцеллюлярной. Содержание воды в
различных тканях и секретах колеблется в очень широких пределах: в скелете-22%,
в печени, мышцах, мозге, сердце, коже и соединительной ткани 70-80%, в плазме
крови 90%, в поте, слюне 99, 5%. Таким образом, вода является основной
составной частью многих тканей и секретов организма.
Обмен веществ тесно
связан с водой. Она является растворителем для большинства соединений и служит
средой, в которой протекают все реакции обмена веществ. Основные процессы, связанные
с обменом веществ (ассимиляция, диссимиляция, диффузия, осмос, резорбция, фильтрация
и другие), протекают только в водных растворах органических и неорганических
веществ. В водной среде осуществляются пищеварение и усвоение пищи в
желудочно-кишечном тракте, транспортировка питательных веществ к различным
тканям. Вода является непосредственным участником процессов окисления, гидролиза
и других реакций обмена. Она необходима для выведения различных вредных веществ,
образующихся в результате обмена. В связи с этим при недостаточном поступлении
воды возникает интоксикация организма. Испаряясь с поверхности кожных покровов
и дыхательных путей, она играет важную роль в процессах терморегуляции
организма.
Вода участвует в обмене
веществ, непрерывно выделяется из организма через почки, легкие, кишечник и
кожу (готовые железы).
При дефиците воды
наступает расстройство многих физиологических функций организма: нарушается
обмен веществ, нарастает количество молочной кислоты, в тканях снижаются окислительные
процессы, увеличивается вязкость крови, повышается температура тела, учащается
дыхание и резко снижается аппетит.
Вода в организме
выполняет механическую роль, облегчая скольжение трущихся поверхностей (суставы,
связки, серозные и слизистые покровы.
Загрязнение поверхностных
вод
Поверхностные водные
системы — ручьи, реки, озера, пруды
— загрязняются в основном
бытовыми промстоками. На чистоту поверхностных вод в сельской местности влияют стоки,
смывающие с полей, ядохимикаты, удобрения, а зачастую бытовой мусор и навоз из
сел и ферм. Качество воды большинства водных объектов не отвечает нормативным
требованиям. Многолетние наблюдения за динамикой качества поверхностных вод
обнаруживают тенденцию увеличения числа створов с высоким уровнем
загрязненности (более 10 ПДК) и числа случаев экстремально высокого содержания
(Свыше 100 ПДК) загрязняющих веществ в водных объектах.
Состояние водных
источников и систем централизованного водоснабжения не может гарантировать
требуемого качества питьевой воды, а в ряде регионов (Южный Урал, Кузбасс, некоторые
территории Севера) это состояние достигло опасного уровня для здоровья
человека. Службы санитарно-эпидемиологического надзора постоянно отмечают
высокое загрязнение поверхностных вод.
Около 1/3 всей массы
загрязняющих веществ вносится в водоисточники с поверхностными и ливневыми
стоками с территории санитарно неблагоустроенных населенных мест, сельскохозяйственных
объектов и угодий, что влияет на сезонное, в период весеннего паводка, ухудшение
качества питьевой воды. В связи с этим проводится гиперхлорирование питьевой
воды, что, однако небезопасно для здоровья населения в связи с образованием
хлорорганических соединений. Наиболее распространенными загрязняющими
веществами поверхностных вод остаются нефтепродукты, фенолы, легкоокисляемые
органические вещества, соединения металлов, аммонийный и нитридный азот.
Основным источником загрязнения являются сточные воды различных производств, предприятий
сельского и коммунального хозяйства, поверхностный сток.
Из-за нестабильной работы
большинства предприятий, их тяжелого финансового положения, а также
неудовлетворительного бюджетного финансирования выполнение водоохранных
мероприятий в стране ведется крайне низкими темпами.
Неблагополучное состояние
малых рек, особенно в зонах крупных промышленных центров, из-за поступления в
них с поверхностным стоком и сточными водами больших количеств загрязняющих
веществ. Значительный ущерб малым рекам наносится в хозяйственной деятельности
из-за нарушения режима хозяйственной деятельности в водоохранных зонах и
попадания в водотоки органических и минеральных загрязнении, а также смыва
почвы в результате водной эрозии.
Огромное количество
загрязняющих веществ вносится в поверхностные воды со сточными водами
предприятий черной и цветной металлургии, химической, нефтехимической, нефтяной,
газовой, угольной, лесной и целлюлозно-бумажной промышленности, предприятий
сельского и коммунального хозяйства, поверхностным стоком с прилегающих
территорий. Существенное влияние оказывают сельскохозяйственные угодья, а так
же пастбища и животноводческие фермы.
Размеры бытовых городских
стоков, подобно промышленности, сбрасываемые в канализацию. Концентрация
органических веществ в этих отходах зачастую выше, чем в бытовых. Особенно
много сточных вод образуется на бойнях, молочных фермах, пивоваренных и винных
заводах, кондитерских фабриках. За счет загрязнения промышленными водами
ослабляется жизнедеятельность организмов. Сточные воды промышленных, кожевенных
предприятий и текстильных фабрик не только отравляют воду но и расходуют
содержащийся в ней кислород. Сточные воды каменоломен делают воду мутной, в
результате ухудшается проникновение света, а в связи с этим падает
биологическая продукция кислорода. Современный уровень очистки сточных вод
таков, что даже в водах, прошедших биологическую очистку, содержание нитратов и
фосфатов достаточно для интенсивного эвтрофирования водоемов.
Эвтрофикация – обогащение
водоема биогенами, стимулирующее рост фитопланктона. От этого вода мутнеет, гибнут
бентосные растения, сокращается концентрация растворенного кислорода, задыхаются
обитающие на глубине рыбы и моллюски.
Под загрязнением водоемов
понимают снижение их биосферных функций и экологического значения в результате
поступления в них вредных веществ. Загрязнение вод проявляется в изменении
физических и органолептических свойств, увеличение содержание сульфатов, хлоридов,
нитратов, токсичных тяжелых металлов, сокращение растворенного в воде кислорода
воздуха, появление болезнетворных бактерий и других загрязнителей
Россия обладает одним из
самых высоких водных потенциалов в мире. На каждого жителя России приходится
свыше 30 000 м³/год воды. Однако в настоящее время из – за загрязнения или
засорения около 70% рек и озер России утратили свои качества питьевого
водоснабжения, в результате около половины населения потребляют загрязненную
воду. Установлено, что более 400 видов веществ могут вызвать загрязнение вод.
В случае превышения нормы
допустимой хотя бы по одному из трех показателей вредности: санитарно –
токсикологическому, общесанитарному или органолептическому, вода считается
загрязненной.
Различают естественные и
антропогенные источники загрязнения вод. Первые в отличие от вторых
сбалансированы процессами самоочищения вод за счет круговорота веществ в
природе. Этим механизмом природа пользуется в течение всей истории
существования биосферы. Антропогенные загрязнения связано с хозяйственной
деятельностью человека. Сюда относят биологическое, химическое и физическое
загрязнение.
Биологическое загрязнение
вызывается микроорганизмами и способными к брожению органическими веществами.
Такое загрязнение приводит к бактериологическому заражению (инфекционный
гепатит, холера, тиф, дизентерия, кишечная инфекция). Здесь возникает проблема
гигиены.
Бактериологические
показатели питьевой воды. Питьевая вода не должна содержать болезнетворных
микробов. Санитарным показателем качества воды по ГОСТ 2874- является титр
(колититр) кишечной палочки, т. е наименьшее количество воды, в которой
обнаруживается одна кишечная палочка.
Для водопроводной воды
титр 300. это означает, что в 300 мл воды допускается 1 кишечная палочка.
Определяется индекс
кишечной палочки (наименьшее количество кишечных палочек в 1л воды). Для
водопроводной воды он должен равняться 3м. Большое количество их указывает на
возможность попадания в воду болезнетворных микробов, которые вызывают кишечное
инфекционное заболевание.
Общее количество микробов
в воде так же служит показателем её санитарного качества. В одном мл питьевой
воды по ГОСТ 2874-82 «вода питьевая допускается не более 100 микробов».
Источниками загрязнения
органикой являются пищевые предприятия, молочные сахарные заводы, сыроварни, животноводство
и т.д. Например, один целлюлозно-бумажный комбинат загрязняет воду, что и город
с населением 500 тыс. человек. Химическое загрязнение природных вод
представляет собой изменение естественных химических свойств воды за счет
увеличения в ней вредных примесей как неорганической (минеральные соли, кислоты,
щелочи, глиняные частицы) так и органической природы (нефть, нефтепродукты, ПАВ,
пестициды).
Органическое загрязнение
обычно оценивается биохимическим потреблением кислорода БПК 5, 10, 25 суток.
Это, позволяет определить какое, количество кислорода необходимо организмам –
деструкторам для полной минерализации всего нестойкого органического вещества, содержащегося
в 1л воды в течение 5-10 или 25 суток .
Вынос в гидросферу
органического вещества оценивается в 300-380 млн. т. Сточные воды, содержащие
суспензии органического происхождения или растворенное органическое вещество, пагубно
влияют на состояние водоемов. Осаждаясь, суспензии заливают дно и задерживают
развитие или полностью прекращают жизнедеятельность донных микроорганизмов, участвующих
в процессе самоочищения вод. При гниении донных осадков могут образовываться
вредные соединения и отравляющие вещества, такие как сероводород, которые
приводят к полному загрязнению воды в реке. Наличие суспензий затрудняет так же
проникновение света на глубину и замедляет процессы фотосинтеза.
Значительный объем
органических веществ, большинство которых не свойственно природным водам, сбрасывается
в реки вместе с промышленными и бытовыми стоками. Нарастающие загрязнения
водоемов и водостоков наблюдается во всех промышленных странах.
Хлориды: в воде могут
быть минерального и органического происхождения. В некоторых зонах повышенное
содержание их в воде (до 100-300 мг/л) связано с засоленностью грунтов, богатых
хлористыми соединениями. Такая вода не является опасной в санитарном отношении
и пригодна для поения животных и хозяйственных целей.
В питьевой воде
содержание хлоридов органического происхождения не должно превышать 20-30 мг/л.
при отсутствии других загрязнений в воде допускается содержание хлоридов
минерального происхождения до 350мг/л. вода, в которой хлоридов содержится
более 500 мг/л, имеет солоноватый привкус и неблагоприятно влияет на желудочную
секрецию.
Питьевая вода при
содержании хлоридов 500 мг/л и выше усиливает эвакуаторную деятельность желудка
и уменьшает количество, кислотность и переваривающую способность желудочного
сока, что приводит к нарушению процессов пищеварения. При длительном
потреблении воды с наличием хлоридов в количестве 1.0- 2.5г/л у животных
изменяются некоторые показатели водно-солевого обмена, повышается артериальное
давление и наблюдается расстройство пищеварения.
Сульфаты: (соли серной
кислоты) могут быть в воде органического происхождения, что свидетельствует о
ее загрязнении. Однако в некоторых зонах в воде содержится большое количество
(до 2000-3000 мг/л) сульфатов минерального происхождения. Они придают воде
горький вкус и вызывают расстройства деятельности желудочно-кишечного тракта
(обладают слабительным действием, угнетают деятельность желудочных желез и
др.). оптимальное содержание сульфатов в воде составляет около 50 мг/л. однако
при отсутствии других показателей загрязнения допускается наличие в воде
сульфатов минерального происхождения до 500 мг/л.
Активная реакция или рН:
обуславливают наличием в ней органических солей животного и растительного
происхождения, процессами их гниения, а так же содержанием минеральных веществ.
Вода хорошего качества чаще всего нейтральной реакции, а иногда слабощелочной
рН (6.5-8.5). Если в воде повышено содержание органического происхождения, а
тем более имеются процессы животного происхождения, гниения, то она приобретает,
кислую реакцию. Повышенное содержание солей, жесткость воды способствует
сдвигам к щелочной реакции.
Неорганическое
загрязнение. Основными неорганическими (минеральными) загрязнителями пресных и
морских вод являются разнообразные химические соединения, токсичные для
обитателей водной среды. Это соединение свинца, кадмия, ртути, хрома, меди, фтора.
Большинство из них попадают в воду в результате человеческой деятельности.
Тяжелые металлы поглощаются фитопланктоном, а затем передаются по пищевой цепи
организмом. Среди основных источников загрязнения гидросферы минеральными
веществами и биогенными элементами следует упоминать предприятия пищевой промышленности
и сельского хозяйства. Например, с орошаемых земель ежегодно вымывается около
12 млн.т солей.
В связи с быстрыми
темпами урбанизации и несколько замедленным строительством очистных сооружений
водные бассейны и почва загрязняются бытовыми отходами. Особенно ощутимо
загрязнение в водоемах с замедленным течением или непроточным (водохранилища, озера).
Ежегодно в реки сбрасывается около 160 км³ промышленных стоков, а так как
большая часть сточных вод не очищается или очищается недостаточно, то они загрязняют
4000 км³ речных вод – более 12% всего речного стока.
Значительных размеров
достигает концентрация загрязнений дождевых сточных вод – ливневых и талых.
Текущие по улицам дождевые стоки бывают более ядовитыми, чем в сточных трубах
промышленных предприятий. Попадая через канализационную сеть в открытые водоемы
эти стоки отравляют природные воды.
Физическое загрязнение.
Связано со сбросом тепла в воду, что приводит к потрясению всего биоценоза
водоема. К физическим относят также радиоактивное загрязнение вод, попадание в
водные системы различных взвесей, что приводит к изменению прозрачности воды.
Неприятный запах, вкус так же относят к физическому загрязнению.
Источником теплового
загрязнения служат подогретые сбросные воды теплоэлектростанций и промышленности.
Повышение температуры природных вод изменяет естественные условия для водных
организмов, снижает количество растворенного кислорода, изменяет скорость
обмена веществ.
Прозрачность: воды
зависит от наличия или отсутствия в ней взвешенных частиц различных веществ.
Вода хорошего качества должна иметь прозрачность не менее 25 см, через который свободно читается шрифт Снеллена. Большая мутность воды (как от повышенной
концентрации взвешенных минеральных и органических веществ, так и от
растворенных в воде солей) нередко требует специальных методов обработки, улучшающих
её качество.
Cточные воды и санитарные условия спуска сточных
Сточными называются воды,
которые были использованы для тех или иных нужд и получили при этом
дополнительные примеси (загрязнения), изменившие их первоначальный химический
состав и физические свойства.
В зависимости от
происхождения, вида и качественной характеристики примесей сточные воды
подразделяются на три основные категории: бытовые (хозяйственно-фекальные);
производственные (промышленные); атмосферные или дождевые.
Состав и свойства воды, водных
объектов должны контролироваться в створе, расположенном на водотоках на 1 км выше ближайших по течению пунктов водопользования (водозабор для хозяйственно-питьевого
водоснабжения, места купания, организованного отдыха, населенные пункты и тому
подобное), а на непроточных водоемах и водохранилищах – на 1 км в обе стороны от пункта водопользования.
Запрещается сбрасывать в
водные объекты сточные воды, содержащие возбудителей инфекционных заболеваний.
Сточные воды, опасные в эпидемическом отношении, могут сбрасываться в водные
объекты только после соответствующей очистки и обеззараживания.
Запрещается сброс в
водные объекты, на поверхность ледяного покрова водосбора пульпы, концентрированные
кубовые остатки образующееся в результате обезвреживания сточных вод, в том
числе содержащие радионуклиды, другие технологические и бытовые отходы.
Сброс сточных вод в
водные объекты в черте населенных пунктов запрещается.
Место выпуска сточных вод
должно быть расположено ниже по течению реки от границы населенного пункта и
всех мест водопользования населения с учетом возможности обратного течения при
нагонных ветрах.
Сброс сточных вод в
водные объекты в черте населенного пункта через существующие выпуски
допускается лишь в исключительных случаях при соответствующем
технико-экономическом обосновании и по согласованию с органами государственного
санитарного надзора. В этом случае нормативные требования, установленные к
составу и свойствам воды водных объектов, должны быть отнесены к самим сточным
водам.
Условия отведения сточных
вод в водные объекты определяются с учетом: а) степени возможного смещения и
разбавления сточных вод водой водного объекта на участке от места выпуска
сточных вод до расчетных (контрольных) створов ближайших пунктов
хозяйственно-питьевого, культурно-бытового водопользования населения; б)
фонового качества воды водного объекта выше места рассматриваемого выпуска
сточных вод по анализам не более двухлетней давности; при наличии других –
существующих и (или) проектируемых – выпусков сточных вод между рассматриваемым
и ближайшим пунктом водопользования в качестве фонового применяется уровень
загрязнения воды водного объекта с учетом вклада указанных выпусков сточных
вод; в) нормативов качества воды водных объектов (ПДК).
Виды
очистки сточных вод
Строительство очистных
сооружений предусматривается в полном объеме с полной механической и
биологической очисткой сточных вод.
На сооружениях
механической очистки происходит осветление сточной жидкости за счет удаления из
нее крупных взвесей, песка, жира и других нерастворимых веществ, путем пропуска
через решетки и отстаивания при малых скоростях притока.
В состав сооружений
механической очистки входят: решетки, песколовки с круговым движением сточных
вод и первичные отстойники.
Состав сооружений
биологической очистки:
Аэротенки предназначенные
для биологического окисления органических веществ с помощью активного ила и
продуваемого через сточную жидкость воздуха;
вторичные отстойники, которые
служат для задержания ила после аэротенков.
В биологической очистке
выделяют следующие стадии.
На первой стадии, сразу
же после смешения сточных вод с активным илом, на его поверхности происходят
адсорбция загрязняющих веществ и их коагуляция (укрупнение частиц несущих
органические вещества), причем адсорбция обеспечивается как хемосорбцией, так и
биосорбцией с помощью полисахаридного геля активного ила и благодаря огромной
поверхности ила, один грамм которого занимает 100 м2. Таким образом, на первой стадии очистки, загрязняющие вещества в сточных водах удаляются
благодаря механическому изъятию их активным илом из воды и началу процесса
биоокисления наиболее легкоразлагающейся органики. На первой стадии за 0, 5-2, 0
часа содержание органических загрязняющих веществ, характеризуемых показателем
БПК5, снижается на 50-60%
На второй стадии
продолжается биосорбция загрязняющих веществ и идет их активное окисление
экзоферментами (ферментами, выделяемыми активным илом в окружающую среду).
Благодаря снизившейся концентрации загрязняющих веществ, начинает
восстанавливаться активность ила. Продолжительность этой стадии составляет от 2,
0 до 4, 0 часов.
На третьей стадии очистки
происходит окисление загрязняющих веществ эндоферментами (внутри клетки), доокисление
сложноокисляемых соединений, превращение азота аммонийных солей в нитриты и
нитраты, регенерация активного ила. Именно на этой стадии (стадии
внутриклеточного питания активного ила) происходит образование полисахаридного
геля, выделяемого бактериальными клетками. Продолжительность третьей стадии от
4-6 часов при очистке бытовых сточных вод и может удлиняться до 15 часов для
сточных вод сложного промышленного состава.
§
2 Исследовательская часть
Исследования проводили в
лаборатории МУП «Водоканал» г. Тотьма.
Материалом для
исследований служили пробы сточных вод, сбрасываемых в систему канализации г.
Тотьма, и очищенных сточных вод до и после сброса в р. Сухона. Отбор проб
проводили в соответствии с требованиями ГОСТ РФ 5.592-2000 «Вода. Общие
требования к отбору проб».
Результаты анализа сравнивали
с перечнем ПДК вредных веществ в водных объектах согласно СанПиН 2.1.5.980-00.
«Гигиенические требования к охране поверхностных вод» и нормативами ПДС
загрязняющих веществ в р. Сухона.
Для определения качества
речой воды и степени очистки сточных вод путем определения контролируемых
показателей были выбраны из числа органолептических – прозрачность, запах, цветность;
из гидрохимических - взвешенные вещества, водородный показатель (рН), азот
аммония, нитраты, нитриты, фосфаты, сульфаты, хлориды, биохимическое
потребление кислорода (БПКполн), содержание растворенного кислорода, перманганатная
окисляемость, тяжелые металлы.
Цветность определяли в
пробе воды после ее центрифугирования фотометрически по 100-градусной
хромово-кобальтовой шкале цветности и выражали в градусах цветности. Степень
прозрачности определяли по высоте столба жидкости в см, через который отчетливо
виден специальный шрифт.
Запах определяли
качественно и описывали как фекальный, гнилостный, керосиновый, фенольный и
т.д. Интенсивность запаха оценивали в баллах по 5-бальной шкале.
Содержание взвешенных
веществ определяли гравиметрическим методом (ПНД Ф 14.1:2.110–97), который
основан на выделении их из пробы фильтрованием воды через мембранный фильтр с
диаметром пор 0, 45 мкм или бумажный фильтр «синяя лента» и взвешивании осадка
на фильтре после высушивания его до постоянной массы.
Концентрацию водородных
ионов (pH) устанавливали потенциометрическим методом с помощью pH-метра. Метод
основан на измерении разности потенциалов, возникающих на границах между
внешней поверхностью стеклянной мембраны электрода и исследуемым раствором, с
одной стороны, и внутренней поверхностью мембраны и стандартным раствором – с
другой. Внутренний стандартный раствор стеклянного электрода имеет постоянную
концентрацию ионов водорода, поэтому потенциал на внутренней поверхности
мембраны не меняется. Измеряемая разность потенциалов определяется потенциалом,
возникающим на границе внешней поверхности электрода и исследуемого раствора.
Концентрацию ионов
аммония определяли методом фотометрии по реакции с реактивом Несслера (ПНД Ф
14.1.1– 95). Принцип метода основан на том, что аммоний с реактивом Несслера
образует йодид меркураммония, который окрашивает раствор в желто-коричневый
цвет. Интенсивность окраски пропорциональна содержанию аммония в воде.
Массовую концентрацию
нитрат-ионов определяли фотометрическим методом с салициловой кислотой (ПНД Ф
14.1:2.4– 95). Фотометрический метод основан на взаимодействии нитрат-ионов с
салициловой кислотой с образованием комплексного соединения желтого цвета.
Содержание нитритов
определяли фотометрическим методом с реактивом Грисса (ПНД Ф 14.1:23–95).
Определение основано на способности нитритов диазотировать сульфаниловую
кислоту и на образовании красно-фиолетового красителя диазосоеденения с α
– нафталамином. Интенсивность окраски пропорциональна концентрации нитритов.
Протекание реакции в значительной степени зависит от pH-среды.
Измерение массовой
концентрации сульфат-ионов проводили турбидиметрическим методом (ПНД Ф
14.1:2.159–2000). Метод измерения массовой концентрации сульфат-ионов основан
на образовании стабилизированной суспензии сульфата бария в солянокислой среде
с последующим измерением светорассеяния в направлении падающего луча ( в
единицах оптической плотности).
Измерение содержания
хлоридов проводили аргентометрическим методом (ПНД Ф 14.1:2.96–97).
Титриметрический метод определения массовой концентрации хлоридов основан на
образовании трудноратворимого осадка хлорида серебра при прибавлении раствора
нитрата серебра к анализируемой воде. После полного осаждения хлоридов избыток
ионов серебра реагирует с индикатором – хроматом калия – с образованием
красновато – оранжевого осадка хромата серебра. Титрование проводят в
нейтральной или слабощелочной среде (pH=7-10), поскольку в кислой среде не
образуется хромат серебра, а в сильнощелочной возможно образование оксида
серебра Ag2О.
Измерение массовой
концентрации фосфат-ионов проводили фотометрическим методом восстановлением
аскорбиновой кислотой ( ПНД Ф 14.1:2.112– 97). Метод определения основан на
взаимодействий фосфат-ионов в кислой среде с молибдатом аммония и образованием
фосфорно-молибденовой гетерополикислоты, которая восстанавливается аскорбиновой
кислотой в присутствии сурьмяно-виннокислого калия до фосфорно-молибденового
комплекса, окрашенного в голубой цвет.
Метод перманганатной
окисляемости основан на окислении органических загрязнений (с помощью кислорода,
который эквивалентен загрязнению) перманганатом калия в мягких условиях при
кипячении, которое проводят только в очищенное воде.
Измерение массовой
концентрации общего железа проводили фотометрическим методом с
сульфосалициловой кислотой (ПНД Ф 14.1:2.50 - 96). Фотометрический метод
определения массовой концентрации общего железа основан на образовании
сульфосалициловой кистой и ее натриевой солью с солями железа окрашенных
комплексных соединений, причем, в слабокислой среде сульфосалициловая кислота
реагирует только с солями железа (3+) (красное окрашивание), а в слабощелочной
среде – солями железа (2+) и (3+) (желтое окрашивание).
Выполнение измерений
биохимического потребления кислорода (ПНД Ф 14.1:2:3:4.123– 97) основано на
способности микроорганизмов потреблять кислород при биохимическом окислении
органических веществ и неорганических веществ в воде. Биохимическое потребление
кислорода определяют количеством кислорода в мг/дм³, которое требуется для
окисления находящихся в воде углеродосодержащих органических веществ в аэробных
условиях в результате биохимических процессов.
Содержание растворенного
кислорода устанавливали йодометрическим методом (ПНД Ф 14.1:2.101– 97), в
основе которого лежит реакция кислорода с гидроксидом марганца (II) в щелочной
среде. Последний количественно связывает кислород, переходя при этом в
соединения марганца (IV). При подкислении пробы в присутствии избытка иодида
калия образуется йод, количество которого эквивалентно содержанию растворенного
кислорода и определяется титрованием раствором тиосульфата натрия .
Концентрацию тяжелых
металлов устанавливали методом атомно-абсорбционной спектрофотометрии. Способ
основан на полном разложении органических веществ путем сжигания пробы сырья
или продукта в электропечи при контролируемом температурном режиме и атомизации
распыленного раствора (ГОСТ 26929-94) [4, 26].
Характеристика
технологических процессов очистки сточных вод
Приемником очищенных
сточных вод является река Сухона. Выпуск сточных вод расположен на правом
берегу реки.
Тотьма канализована
частично. Протяженность главных канализационных коллекторов – 18, 3 км, уличной канализационной сети – 35, 7 км, внутриквартальной канализационной сети – 24, 1 км. На сети расположено 8 канализационных насосных станций, которые перекачивают сточные воды на
главную канализационную насосную станцию (ГКНС), откуда они поступают в
приемную камеру очистных сооружений канализации (ОСК) г. Тотьма.
Сточные воды из выгребов
на очистные сооружения канализации вывозятся ассенизационными машинами. Вывозом
сточных вод занимается МУП «Водоканал» г. Тотьма.
Площадка очистных
сооружений канализации расположена в черте города и имеет полный цикл
механической и биологической очистки сточных вод. Проектная мощность ОСК – 20
тыс. м3/сут., фактическая - 12 тыс. м3/сут.
Сточные воды через
главную канализационную насосную станцию перекачиваются в приемную камеру
очистных сооружений по коллектору диаметром 1000 мм. Камера оборудована аварийным переливным трубопроводом. Из камеры сточные воды поступают по
лоткам в здание решеток, где происходит удаление крупных примесей решеткой
РМУ-2 и агрегатом механической очистки сточных вод ХЖ 2.966.021 ПС (г.
Владимир). Из здания решеток сточные воды, проходя лоток Вентури, поступают на
горизонтальные песколовки с круговым движением воды.
Песколовки предназначены
для выделения тяжелых минеральных примесей из сточной воды. Осадок из
песколовок удаляется гидроэлеваторами и направляется в песковые бункеры (2
бункера), размещенные в пристрое сливной станции, откуда по мере наполнения
вывозится грузовой машиной за пределы станции. Из песколовок сточные воды по
лоткам поступают в распределительные камеры, и подаются на первичные
отстойники.
Первичные отстойники
входят в состав технологических сооружений блока емкостей, состоящего из
нескольких секций шириной 15 м каждая и объединяющего в себе илоперегниватели, аэротенки,
аэробные минерализаторы, вторичные отстойники и контактные резервуары.
Первичные отстойники служат для дальнейшего удаления неосевших в песколовках
минеральных и органических веществ, способных к осаждению путем длительного
отстаивания. Отстойники радиального типа, квадратные в плане (10х10 м), четырехконусные,
без скребковых механизмов. Сточная вода подается в центральную часть отстойника
и собирается периферийным лотком. Выпадающий в отстойнике сырой осадок
удаляется из конусов эрлифтами и направляется в илоперегниватель, где
происходит анаэробное сбраживание осадка. Из первичных отстойников сточная вода
отводится в аэротенки.
Аэротенки предназначены
для биологического окисления органических веществ с помощью активного ила и
воздуха. Аэротенки – двухкоридорные с регенерацией 50 % активного ила. Подача
стоков осуществляется рассредоточено через впускные окна распределительного
лотка. Циркуляционный активный ил подается в аэротенк сосредоточенно.
Распределение воздуха в аэротенках осуществляется дырчатыми полимерными
аэраторами (мелкопузырчатая аэрация).
Пройдя биологическую
очистку, иловая смесь по дюкеру подается в центральную часть вторичного
отстойника, где происходит отделение очищенной воды от ила. Выпадающий ил
удаляется из конусной части эрлифтами и направляется в аэротенк (циркуляционный
ил), избыточный активный ил сбрасывают в аэробный минерализатор. Аэробные
минерализаторы – сооружения, где происходит аэробное сбраживание избыточного
ила. Воздух распределяется дырчатыми трубами. Для удаления осадка и отделения
иловой воды предусматривается зона отстаивания. Отстоянная жидкость отводится в
регенератор аэротенка. Минерализованный ил насосами перекачивается на иловые
поля.
Из сборного лотка
вторичного отстойника очищенная сточная жидкость поступает в контактный
резервуар. Емкость контактных резервуаров определена из расчета контакта хлора
со сточной водой в резервуаре не менее 30 минут. Обеззараживание не
производится.
Иловые поля – площадки –
уплотнители, представляют собой железобетонные резервуары, в которые осадок
98%-й влажности подается по лотку. После отстаивания иловая вода выпускается
через отверстия, снабженные шиберами и расположенные в продольной стенке
уплотнителя на разных глубинах в открытый лоток, размещенный в продольной
галерее. Из галереи иловая вода поступает самотеком в сеть и подается иловой
насосной станцией на полный цикл очистки. Осадок складируется на иловые поля
очистных сооружений. Иловый осадок нетоксичен и относится к 5 классу опасности.
Эксплуатируемые очистные
сооружения находятся в аварийном состоянии, требуют капитального ремонта и
реконструкции.
Характеристика
поступающих на очистку сточных вод
При оценке сточных вод, сбрасываемых
в водоемы, большое внимание уделяется органолептическим и физико-химическим
показателям.
Одним из таких
показателей является прозрачность сточных вод, мерой которой служит высота
столба воды, при которой сквозь нее можно читать шрифт определенного размера и
типа. Хозяйственно-бытовые сточные воды поступающие на очистку должны иметь
прозрачность не менее 10 см. Прозрачность сточной воды обусловлена наличием в
ней нерастворенных и коллоидных примесей.
Результаты
органолептических исследований представлены в таблице 1.
1. Органолептические
показатели сточных вод
| Показатель |
Сезон
года |
Норматив
(СанПиН
2.1.5.980-00)
|
| Зима |
Весна |
Лето |
Осень |
| Прозрачность,
см |
2 |
7 |
5 |
6 |
Не
< 10 |
| Запах,
балл |
5 |
5 |
5 |
5 |
Не
> 5
(обнаруживаемый
непосредственно)
|
| Цвет |
Серый
(11 см)
|
Серый
(6 см)
|
Серый
(8 см)
|
Серый
(11 см)
|
Не
должен обнаруживаться в столбике 10 см |
Из данных таблицы видно,
что сточные воды, поступающие на очистку, имели прозрачность 2 – 7 см на протяжении всего периода исследований. Самыми прозрачными сточные воды были в весенний, наиболее
мутными – в зимний период. Значение данного показателя во всех исследованных
пробах не соответствовало требованиям СанПиН. По запаху не наблюдалось
отклонений от нормативных требований.
Серый цвет соответствует
хозяйственно-бытовым сточным водам, однако окраска не должна обнаруживаться в
столбике глубиной 10 см. Весной и летом сточные воды имели цветность выше
требуемой на 40 и 20 % соответственно.
Одним из значимых
факторов, воздействующих на скорость изъятия загрязняющих веществ при
механическом отстаивании, интенсивность обмена веществ у организмов активного
ила, потребление растворенного кислорода, а следовательно, на эффективность
процесса биохимического окисления, является температура очищаемой сточной воды.
Существенное воздействие температуры на процесс очистки наблюдается при
отсутствии горячего водоснабжения. Оптимальные значения для удовлетворительного
процесса биологической очистки находятся в диапазоне 16 - 23˚С. От
температуры сточной воды зависит эффект первичного отстаивания. С повышением
температуры степень содержания взвешенных веществ увеличивается от 5 до 10%.
Работа вторичных отстойников ухудшается зимой на 20 – 30% в связи с понижением
температуры воды, поступающей на очистку.
2. Физико-химические
показатели сточных вод
| Показатель |
Сезон года |
ПДК |
| Зима |
Весна |
Лето |
Осень |
| Температура, ˚С |
17 |
21 |
23 |
20 |
16, 0 – 23, 0 |
| рН |
7, 8 |
7, 3 |
7, 9 |
8, 1 |
6, 5 – 8, 5 |
Результаты исследований
показали, что температура поступающей сточной воды в весенний, летний и осенний
сезоны года не имела отклонений от оптимальных величин. При оптимальной реакции
среды это является очень важным условием для успешной очистки сточных вод.
Однако необходимо отметить, что минимальное значение температуры (17˚С)
наблюдалось в зимний период и было на уровне нижнего предела требуемой величины,
максимальное – в летний (23˚С).
Концентрацию водородных
ионов сточных вод необходимо определять потому, что стоки канализации имеют
кислую реакцию. В результате чего создается опасность гибели микроорганизмов биологической
пленки, а после сброса таких стоков в водоем возникает угроза гибели в нем
флоры и фауны, снижения его самоочищающей способности.
При рН 6, 0
жизнедеятельность микроорганизмов на биологических фильтрах снижается, а при рН
менее 5, 0 в ряде случаев прекращается совсем .
Как показывают данные
таблицы 2, рН сточных вод во все исследуемые периоды составил 7, 3 – 8, 1, что
соответствует значению ПДК.
Среди основных
загрязняющих веществ, прежде всего органической природы, присутствующих в
сточных водах очистных сооружений, по физическому состоянию (размеру
составляющих частиц), выделяют соединения в нерастворенном, коллоидном и
растворенном состояниях. По мере изменения степени дисперсности частиц загрязняющих
веществ происходит последовательное их изъятие на всех ступенях биологической
очистки. Среди них для характеристики работы сооружений механической очистки
большое значение имеют взвешенные вещества, т.е. частицы нерастворимого
твердого вещества, плавающие по всему объему жидкости (грубые суспензии). Они
являются показателем загрязнения водоема хозяйственно-бытовыми сточными водами.
3. Содержание взвешенных
и оседающих веществ в сточных водах, мг/дм3
| Показатель |
Сезон года |
ПДК |
| Зима |
Весна |
Лето |
Осень |
| Взвешенные
вещества |
32, 39±0, 90 |
56, 43±1, 50 |
21, 94±0, 80 |
36, 58±1, 10 |
10, 45 |
| Оседающие
вещества |
22, 02±1, 30 |
39, 50±1, 50 |
15, 36±1, 20 |
26, 70±1, 10 |
6, 79 |
Содержание взвешенных
веществ в сточных водах во все периоды года превышало допустимую концентрацию в
3, 1; 5, 4; 2, 1; 3, 5 раза по сезонам соответственно. Это означает, что
степень очистки сточных вод по взвешенным веществам после аэротенков и
биофильтров неудовлетворительна. В аротенках наблюдаются буруны, что говорит о
необходимости замены системы аэрации, так как неравномерная подача воздуха в
аротенки приводит к ухудшению качества очистки и лишнему расходу воздуха .
При анализе сезонной
динамики содержания взвешенных веществ в сточных водах системы канализации г.
Тотьма установлено, что наибольший уровень их зарегистрирован в весенний период
(56, 43±2, 50 мг/дм3), что было выше в 1, 74 раза, чем зимой, в 2, 57; 1, 54
раза - по сравнению с летним и осенним периодами соответственно.
Необходимость определения
содержания этой группы веществ в сточных водах обусловлена присутствием в них
одного из наиболее вредных взвешенных веществ органического происхождения
лигнина. Большая часть его извлекается из сточных вод в процессе очистки. При
высоких концентрациях взвешенных веществ в сточных водах лигнин на очистных
сооружениях, как правило, не полностью выпадает в осадок в отстойниках и может
поступать со сточными водами в водоемы. Попадая в жабры рыб, лигнин вызывает их
закупорку, затрудняет дыхание и приводит к гибели рыбы.
Для характеристики работы
сооружений механической очистки большое значение имеет содержание не только
взвешенных, но и количество оседающих веществ. Оседающие вещества – это часть
взвешенных веществ, выпадающих в осадок за 2 ч отстаивания в лабораторном
цилиндре; они рассчитываются по объему (см/дм3) и весу (мг/ дм3).
Из данных таблицы 3 видно,
что уровень содержания оседающих веществ максимальным был весной, в другое
время года он снижался: осенью – в 1, 48, летом – в 2, 57, зимой – в 1, 79
раза. Все эти значения превышали ПДК в 3, 24; 5, 82; 2, 26; 3, 9 раза за год.
Количество оседающих
веществ, выраженное в процентах от количества взвешенных, - это теоретически
возможный предел эффективности отстаивания взвеси в условиях первичных
отстойников. В бытовых неочищенных сточных водах оседающие вещества составляют
65 – 75% взвешенных по массе. Это не подтверждается нашими исследованиями и
свидетельствует, во-первых, о высокой степени загрязненности
хозяйственно-бытовых сточных вод, прежде всего, органическими соединениями, во-вторых,
что очень важно, указывает на возможность не полного отстаивания взвеси в
условиях первичных отстойников.
Перед сооружениями
биологической очистки ставится задача глубокого удаления всех форм
азотсодержащих соединений. В сточных водах азот представлен, в основном, в виде
минеральной (NH4+ , NО2-, NО3-) и органической (аминокислоты и др. органические
соединения) составляющих.
4. Содержание азота в
сточных водах, мг/ дм3
| Показатель |
Сезон года |
ПДК |
| Зима |
Весна |
Лето |
Осень |
| Азот аммонийный |
0, 51±0, 03 |
0, 80±0, 01 |
0, 88±0, 05 |
0, 56±0, 02 |
0, 40 |
| Нитриты |
0, 18±0, 02 |
0, 27±0, 01 |
0, 41±0, 03 |
0, 28±0, 02 |
0, 08 |
| Нитраты |
12, 96±0, 92 |
20, 64±0, 85 |
21, 27±0, 79 |
11, 04±0, 67 |
40, 00 |
Как показывают данные
таблицы 4, наибольшее поступление азота аммонийного наблюдалось в летний период
(0, 88±0, 13 мг/ дм3), в другие периоды года оно снижалось: осенью – в 1, 57
раз, весной – на 10 %, зимой – в 1, 57 раз. В первом квартале года значение
этого показателя было самым невысоким и превышало ПДК на 7, 5%, тогда как
осенью оно превышало ПДК на 27, 5 %; весной – в 2 раза; летом – в 2, 2 раза.
Аммонийный азот в большом количестве образуется при гидролизе мочевины —
продукта жизнедеятельности человека. Процесс аммонификации белковых соединений
приводит к образованию аммония. Следовательно, в теплое время года в сточные
воды поступает большее количество фекалий, в том числе и из выгребных ям.
В хозяйственно-бытовых
сточных водах до их очистки азот в окисленных формах — нитриты и нитраты — как
правило, отсутствует. Окисленные формы азота отсутствуют даже в том случае, если
в производственных стоках имелись нитриты и нитраты. Денитрификация примесей
сточной воды объясняется процессами анаэробиоза при транспортировании сточных
вод по системе водоотведения, действием бактерий, денитрифицирующих окисленные
формы азота до молекулярной формы. Окисленные формы азота появляются после
биологической очистки сточных вод, свидетельствуя о полной завершенности
процесса.
Азот служит питательной
средой для многих микроорганизмов, применяемых при биологической очистке в
аэротенках и необходим для нормальной работы биологической пленки очистных
канализационных сооружений. В случае его значительного количества в сточных
водах, а также после биологической очистки и разбавления в водоеме его
содержание увеличивается, усиливается разрастание сине-зеленых водорослей (цветение
воды), что часто наблюдается в летний период.
Содержание нитратов во
все исследуемые периоды в сточных водах находилось в пределах нормативных
значений. Самым высоким оно было также в летний, самым низким – в зимний период,
весной и осенью занимало промежуточное значение.
Концентрация нитритов в
течение всего года превышала ПДК: зимой – в 1, 8; весной – в 2, 9; летом – в 4;
осенью – в 2, 8 раза, что является признаком промышленных загрязнений стоков
канализации г. Тотьма и нарушения технологии биологической очистки сточных вод.
Хлориды и сульфаты —
примеси сточных вод, не влияющие на скорость и эффективность процесса очистки, если
их концентрация невелика; при этом их концентрация в сточных водах не
изменяется. Хлориды не влияют на биохимические процессы даже при концентрациях
10 г/л, но во избежание засоления воды водоемов — приемников сточных вод
следует предотвращать сброс высокоминерализованных производственных сточных вод
в поселковую систему водоотведения.
Концентрация сульфатов
может изменяться лишь в анаэробных условиях при очистке сточных вод в
двухъярусных отстойниках и сбраживании осадка в метантенках. В этих процессах
сульфаты восстанавливаются до сульфидов и при концентрации более 1 г/дм3 могут
нарушать процесс метанового брожения.
5. Содержание анионов в
сточных водах, мг/дм3
| Показатель |
Сезон года |
ПДК |
| Зима |
Весна |
Лето |
Осень |
| Сульфаты |
124, 2±12, 3 |
178, 1±4, 5 |
235, 8±18, 2 |
190, 65±2, 9 |
500, 0 |
| Хлориды |
52, 3±0, 7 |
115, 0±9, 4 |
264, 6±10, 8 |
121, 6±5, 1 |
300, 0 |
| Фосфаты (по
фосфору) |
1, 34±0, 01 |
2, 38±0, 01 |
3, 3±0, 01 |
1, 56±0, 02 |
0, 2 |
Как показывают
результаты исследований, представленные в таблице 5, содержание сульфатов в
сточных водах в течение всего периода наблюдений находилось в пределах 78, 1-
235, 8 мг/дм3 при ПДК 500 мг/дм3 (СанПиН 2.1.5.980 - 00) . Концентрация
хлоридов имела значительно больший диапазон колебаний (52, 3- 264, 6 мг/дм3), но
также не превышала допустимой величины. При изучении сезонной динамики данных
показателей установлено, что максимальные их значения установлены в летний
период, минимальные – в зимний, весной и осенью – удерживались примерно на
одном уровне.
Источником фосфора в
сточных водах являются физиологические выделений людей, отходы хозяйственной
деятельности человека и некоторые виды производственных сточных вод. Содержание
азота и фосфора в сточных водах характеризует качество процесса биологической
очистки. Азот и фосфор — компоненты материала клеток микроорганизмов. Их
называют биогенными элементами, при отсутствии азота и фосфора в сточных водах
процесс биологического окисления примесей сточной воды невозможен. На очистных
сооружениях фосфаты применяют в технологии производства для выращивания дрожжей,
а также для нормальной работы биологической пленки очистных сооружений. При
поступлении сточных вод для предварительной механической очистки в отстойнике
концентрация фосфатов заметно задерживает осаждение взвешенных веществ.
Данные таблицы 5
показывают, что содержание фосфатов, поступающих со сточными водами на очистку,
превышает ПДК. При допустимой величине 0, 2 мг/дм3, концентрация фосфатов
составила летом 3, 3 мг/дм3, что выше ПДК в 16, 5 раз. Зимой, весной и осенью
значение этого показателя понижалось, но также оставалось значительно выше
критического уровня в 6, 7; 11, 9; и 7, 8 раз соответственно.
Наиболее полную
информацию о загрязненности сточных вод легкоокисляемыми органическими
веществами возможно получить только после определения БПК в натуральной
(взболтанной) пробе. БПК пробы сточных вод — кислородный эквивалент степени
загрязненности сточных вод биохимически окисляемыми органическими веществами.
БПК устанавливает количество кислорода, необходимое для жизнедеятельности
микроорганизмов, участвующих в окислении и деструкции органических соединений
примесей сточной воды. БПК характеризует часть органических примесей, окисляемых
биохимически и находящихся в растворенном и коллоидном состояниях, и часть
примесей во взвешенном состоянии, которая способна расщепляться под действием
экзоферментов.
6. Окислительные свойства
сточных вод, мг/дм3
| Показатель |
Сезон года |
ПДК |
| Зима |
Весна |
Лето |
Осень |
| БПКполн |
4, 8±0, 05 |
29, 1±0, 9 |
52, 7±3, 6 |
4, 9±0, 03 |
6, 0 |
Из данных таблицы 6
видно, что зимой и осенью биохимическое потребление кислорода было в пределах
допустимых величин. Однако весной оно возрастало по сравнению с этими
значениями в 6, 1 раза и превышало допустимое значение в 4, 8 раза. Летом БПК
продолжало расти, что составило 52, 7 мг/дм3. Данное значение было максимальным
за весь период исследований, оно превысило ПДК в 8, 8 раза. Это свидетельствует
о высоком содержании в сточных водах углеродсодержащей органики, окисляющейся
биологическим способом и выполняющей роль активного субстрата для
микроорганизмов.
Бытовые и промышленные
сточные воды являются одним из источников поступления тяжелых металлов в природные
водоемы. Все промышленные примеси, присутствующие в сточных водах, в той или
иной мере неблагоприятно воздействуют на нормальное функционирование и
жизнеспособность активного ила. Особую проблему представляют токсичные
(ядовитые) сточные воды, убивающие активный ил. Сточные воды содержат большое
количество разнообразных токсикантов, из которых можно выделить два основных
типа: ксенобиотики (органические токсины) и тяжелые металлы.
Тяжелые металлы
извлекаются из сточных вод при биологической очистке путем их активной сорбции
илом. Данные по содержанию тяжелых металлов в сточных водах, поступающих на
очистные сооружения, приведены в таблице 7.
7. Содержание тяжелых
металлов в сточных водах, мг/дм3
| Показатель |
Сезон года |
ПДК |
| Зима |
Весна |
Лето |
Осень |
| Железо общее |
0, 120±0, 020 |
0, 190±0, 010 |
0, 350±0, 010 |
0, 270±0, 010 |
0, 100 |
| Никель |
0, 017±0, 001 |
0, 018±0, 001 |
0, 018±0, 001 |
0, 017±0, 001 |
0, 010 |
| Хром |
0, 08±0, 001 |
0, 09±0, 002 |
0, 09±0, 001 |
0, 08±0, 001 |
0, 070 |
Анализ результатов
исследований показал, что содержание тяжелых металлов во все периоды года
превышает ПДК: по железу общему – в 1, 2 – 3, 5 раза, по никелю – 1, 7 – 1, 8 раза,
по хрому – на 35 % весной и летом, зимой и осенью - на 18 %.
Тяжелые металлы - наиболее
распространенная группа токсичных трудноокисляемых загрязнений, присутствующих
в сточных водах. В неочищенных сточных водах металлы представлены
разнообразными химическими соединениями во взвешенной, коллоидной, растворенной
и нерастворенной формах. Некоторые из солей тяжелых металлов, например, меди, цинка,
трехвалентного хрома в щелочной среде выпадают в осадок. Другие, гидролизуясь, значительно
подкисляют сточные воды. Как правило, тяжелые металлы и их соли действуют на
активный ил как токсиканты, угнетая его окислительную способность. Они вызывают
денатурацию ферментов активного ила, это ингибирует их активность и нарушает
проницаемость мембран у организмов ила, что приводит к его гибели .
В процессе биохимической
очистки часть ионов тяжелых металлов аккумулируется илом. При этом происходит
образование комплексов ионов с белком активного ила, следствием чего является, с
одной стороны, накопление соединений металлов в осадках, а с другой - снижение
качества очистки сточных вод, так как сорбированные металлы концентрируются в
активном иле и с возвратным илом неоднократно попадают в аэротенк, где
значительная часть подаваемого кислорода воздуха затрачивается не на
эффективное биологическое окисление загрязнений, а на восстановление свойств
активного ила после токсического повреждающего воздействия. Тяжелые металлы
ингибируют активный ил при концентрациях 1-5 мг/дм3.
Степень удаления тяжелых
металлов в процессе биологической очистки на очистных сооружениях зависит от
природы металла, его начальной концентрации в неочищенных сточных водах, дозы ила,
времени контакта сточных вод с илом и эффективности сорбции соединений металлов,
в которой активно участвует все тот же полисахаридный гель активного ила.
Таким образом, для
предотвращения неудовлетворительной работы очистных сооружений и сохранения качества
водоемов, принимающих сточные воды требуется на первом этапе в лабораториях
очистных сооружений выполнять необходимые анализы по оценке поступающих сточных
вод. Результаты этих анализов служат оперативной информацией для обеспечения
стабильного и удовлетворительного качества очистки в условиях непрерывно
изменяющегося состава поступающих сточных вод.
Характеристика очищенных
сточных вод, поступающих в реку Сухона и оценка эффективности работы МУП «Водоканал»
г. Тотьма
С целью оценки
эффективности работы очистных сооружений г. Тотьма провели анализ качества
очищенных сточных вод, сбрасываемых в реку Сухона, и полученные результаты
сравнили с качественными показателями исходных сточных вод. Результаты
исследований приведены в таблице 8.
По данным таблицы 8 видно,
что по большинству определяемых показателей сточные воды после очистки также не
соответствовали требованиям СанПиН, хотя и произошло некоторое улучшение их
значений. Так, концентрации взвешенных, оседающих веществ, азота аммония, нитритов,
нитратов, сульфатов, хлоридов, фосфатов, БПКполн, , железа общего, никеля и
хрома в сточных водах после очистки снизились на 40, 42, 45, 38, 35, 16, 25, 31,
39, 10, 12, и 11% соответственно. Однако следует отметить, что значения этих
показателей даже после очистки сточных вод превышали предельно допустимые: по
взвешенным веществам – в 2, 11, оседающим веществам – в 2, 21 раз, нитритам – в
2, 25, фосфатам – 7, 4, БПК полн, - 2, 3, железу общему – в 2, никелю – в 1, 5,
хрому – в 8, 6 раза. Прозрачность очищенных сточных вод была меньше
нормативного значения на 0, 9 см, запах обнаруживался непосредственно и его
интенсивность соответствовала 3 баллам при требуемых 2-х баллах. Цвет сточных
вод после очистки был серым и обнаруживался в столбике воды глубиной 10 см, что не удовлетворяет требованиям к очищенным сточным водам. Температура, рН, концентрации
нитратов, ионов аммония, сульфатов, хлоридов находились в пределах допустимых
значений.
8. Показатели качества сточных
вод, поступающих в реку Сухона
| Показатель |
Стадия обработки |
ПДК, норматив
(СанПиН
2.1.5.980-00)
|
| До очистки |
После очистки |
| Прозрачность, см |
5, 000±0, 320 |
9, 100±0, 130 |
Не < 10 |
| Запах, балл |
5 |
3 |
Не > 2
(обнаруживаемый
непосредственно)
|
| Цвет |
Серый (9 см) |
Серый (10 см) |
Не должен
обнаруживаться в столбике 10 см |
| Температура, ˚С |
20, 250±1, 200 |
19, 300±1, 100 |
16, 000 – 23, 000 |
| рН |
7, 780±0, 100 |
6, 900±0, 300 |
6, 500 – 8, 500 |
| Взвешенные
вещества, мг/дм3 |
36, 80±1, 500 |
22, 080±1, 700 |
10, 450 |
| Оседающие
вещества, мг/дм3 |
25, 900±1, 900 |
15, 020±1, 800 |
6, 790 |
| Азот аммонийный,
мг/дм3 |
0, 690±0, 010 |
0, 380±0, 010 |
0, 400 |
| Нитриты, мг/дм3 |
0, 280±0, 010 |
0, 180±0, 010 |
0, 080 |
| Нитраты, мг/дм3 |
16, 50±0, 800 |
10, 720±0, 500 |
40, 000 |
| Сульфаты, мг/дм3 |
182, 200±5, 100 |
153, 000±7, 800 |
500, 000 |
| Хлориды, мг/дм3 |
138, 40±6, 300 |
103, 80±8, 100 |
300, 0 |
| Фосфаты (по
фосфору), мг/дм3 |
2, 140±0, 100 |
1, 480±0, 100 |
0, 200 |
| БПКполн, мг
О2/дм3 |
22, 90±0, 300 |
14, 00±0, 300 |
6, 000 |
| Железо общее, мг/дм3 |
0, 230±0, 001 |
0, 20±0, 002 |
0, 100 |
| Никель, мг/дм3 |
0, 017±0, 001 |
0, 015±0, 001 |
0, 010 |
| Хром, мг/дм3 |
0, 085±0, 001 |
0, 076±0, 001 |
0, 070 |
В целом эффективность
очистки сточных вод следует считать неудовлетворительной. Такое положение в
значительной степени объясняется физической изношенностью технологического
оборудования. Как следствие происходит значительный сброс неочищенных сточных
вод в реку Сухона, что вызывает ухудшение качества воды.
Органолептические и
гидрохимические показатели речной воды
Эффект очистки сточных
вод наиболее быстро и просто оценивается по прозрачности очищенной воды, которая
зависит от качества очистки, а также от наличия в воде мелких, не оседающих за
два часа хлопьев активного ила и диспергированных бактерий. Прозрачность —
наиболее оперативный, чутко реагирующий на нарушения, показатель качества
очистки. Любые, даже незначительные, неблагоприятные изменения в составе
сточных вод и в технологическом режиме их очистки приводят к диспергированию
хлопьев ила, нарушению хлопьеобразования, а, следовательно, к уменьшению
прозрачности очищенной воды.
Биологическая очистка
сточных вод должна обеспечивать не менее 10 см прозрачности очищенной воды. При полной, удовлетворительной биологической очистке прозрачность составляет 30 и
более сантиметров, причем при такой прозрачности все другие санитарные
показатели загрязнения, как правило, соответствуют высокой степени очистки.
Исходя из выше
изложенного, нами проведены исследования по определению прозрачности очищенной
на очистных сооружениях канализации сточной воды до и после сброса ее в реку
Сухона. Из данных, представленных в таблице 9, видно, что в весенний пepиoд
прозрачность воды значительно уменьшается.
Причем, уменьшение
прозрачности регистрируется в речной воде, как до сброса, так и после сброса
сточной воды. Снижение прозрачности, вероятно, связано с тем, что весной с
талыми водами в открытые водоемы попадает большое количество органических и
минеральных примесей в твердом и коллоидном состоянии. После сброса очищенных
сточных вод в реку уменьшалась прозрачность природных вод во все периоды
исследований, весной интенсивность запаха превышала 2 балла (что не
соответствует ПДК). В другие периоды сезонных изменений в запахе и цвете как до
сброса, так и после сброса очищенных сточных вод не обнаружено. Однако окраска
природной воды после сброса очищенных стоков была установлена в столбике воды
меньшей глубины, чем до сброса, что также свидетельствует о загрязнении речной
воды.
9. Органолептические
показатели речной воды
| Показатель |
До сброса |
После сброса |
ПДК |
| Зима |
Весна |
Лето |
Осень |
Зима |
Весна |
Лето |
Осень |
| Прозрачность, см |
19 |
15 |
18 |
18 |
16 |
13 |
15 |
16 |
Не < 10 |
| Запах, балл |
2 |
2 |
2 |
2 |
2 |
3 |
2 |
2 |
Не > 2 |
| Цвет |
Прозрачный
(18)
|
Прозрачный
(15)
|
более 10 см |
В таблице 10
представлены значения температуры озерной воды до и после сброса очищенных
сточных вод.
10. Физико-химические
показатели речной воды
| Показатель |
До сброса |
После сброса |
ПДК |
| Зима |
Весна |
Лето |
Осень |
Зима |
Весна |
Лето |
Осень |
| Температура, ˚С |
2 |
10 |
18 |
8 |
3 |
12 |
20 |
10 |
Не > 28˚С
летом;
не > 8˚С
зимой
|
| рН |
7, 9 |
7, 6 |
7, 8 |
8, 0 |
8, 0 |
7, 7 |
7, 9 |
8, 2 |
6, 5 – 8, 5 |
Согласно полученным
данным, температура воды в реке до и после сброса в нее очищенных сточных вод практически
оставалась на одном и том же уровне с разницей в 1 – 2 ˚С. Активная
реакция среды находилась в пределах допустимых значений со сдвигом в сторону
щелочной среды. Изменения рН природных вод в кислую или щелочную среду свыше
нормативных негативно отражаются на гидробионтах.
Одним из очень важных
показателей при оценке загрязненности водных объектов являются взвешенные
вещества. Из таблицы 11 видно, что концентрация взвешенных веществ в
исследуемой воде до сброса значительно меньше уровня содержания их в пробах
после сброса: зимой – в 1, 5; весной и летом – в 2; осенью – в 3, 1 раза.
Причем содержание взвешенных веществ в речной воде после смешения с очищенными
сточными водами превышало ПДК в 1, 7; 2, 9; 3; 2, 5 раза по сезонам года
соответственно.
11. Содержание взвешенных
веществ в речной воде
| Показатель |
До сброса |
После сброса |
ПДК |
| Зима |
Весна |
Лето |
Осень |
Зима |
Весна |
Лето |
Осень |
| Взвешенные
вещества, мг/дм3 |
7, 10
±0, 90
|
8, 10
±0, 90
|
8, 60
±0, 80
|
8, 40
±0, 50
|
10, 65
±0, 70
|
16, 20
±1, 30
|
17, 20
±1, 10
|
26, 04
±1, 00
|
10, 45 |
| Оседающие
вещества, мг/дм3 |
4, 60
±0, 10
|
5, 50
±0, 30
|
6, 10
±0, 20
|
5, 80
±0, 10
|
7, 14
±0, 70
|
11, 66
±1, 20
|
12, 04
±0, 80
|
19, 00
±0, 90
|
6, 79 |
При изучении сезонной
динамики содержания взвешенных веществ установлено, самой низкой их концентрация
до и после сброса сточных вод была в зимний период, максимальной – в летний, осенью
и весной – занимала промежуточные значения. На этом фоне аналогично изменяются
концентрации оседающих веществ (таблица 11). Более наглядно сезонная динамика
содержания взвешенных веществ в речной воде представлена на рисунках 1 и 2.
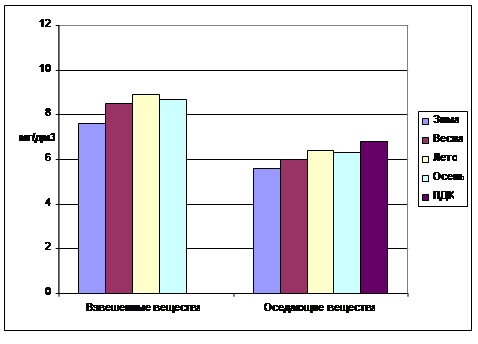
Рис. 1. Сезонная динамика
содержания взвешенных веществ в речной воде до сброса очищенных сточных вод, мг/дм3
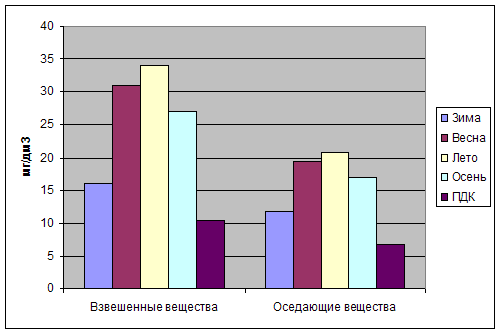
Рис. 2. Сезонная динамика
содержания взвешенных веществ в речной воде после сброса очищенных сточных вод,
мг/дм3
Установленное нами
повышенное количество взвешенных веществ в речной воде после сброса очищенных
сточных вод отрицательно влияет на развитие водной фауны. Взвешенные вещества
минерального происхождения, после очистки, оседают в водоемах на дне, губительно
действуют на бентос, лишая тем самым планктон кормовых ресурсов.
В таблице 12 представлены
данные по содержанию азот включающих примесей в речной воде.
12. Содержание азота в
речной воде до и после сброса очищенных сточных вод, мг/дм3
| Показатель |
До сброса |
После сброса |
ПДК |
| Зима |
Весна |
Лето |
Осень |
Зима |
Весна |
Лето |
Осень |
| Азот аммонийный |
0, 180
±0, 010
|
0, 250
±0, 010
|
0, 310
±0, 010
|
0, 230
±0, 010
|
0, 210
±0, 010
|
0, 300
±0, 010
|
0, 340
±0, 010
|
0, 260
±0, 010
|
0, 400 |
| Нитриты |
0, 020
±0, 001
|
0, 030
±0, 001
|
0, 040
±0, 001
|
0, 030
±0, 005
|
0, 030
±0, 001
|
0, 050
±0, 001
|
0, 070
±0, 001
|
0, 060
±0, 001
|
0, 080 |
| Нитраты |
7, 630
±0, 200
|
8, 240
±0, 200
|
12, 110
±0, 100
|
7, 980
±0, 400
|
7, 60
±0, 500
|
8, 520
±0, 800
|
12, 550
±0, 600
|
8, 140
±1, 100
|
40, 000 |
Как показывают
результаты исследований, до места спуска сточных вод в речной воде в течение
года содержится небольшое количество аммиака. Самые высокие его концентрации
отмечены в весеннее - летний период, самые низкие – зимой. В течение всего года
значения данного показателя не превышали ПДК, т.е. вода здесь не загрязнена.
Уровень содержания аммонийного азота в речной воде после сброса очищенных
стоков увеличивается и становится максимальным в летний период. Весной его
концентрация становилась еще ниже. Повышение содержания аммиака в теплые сезоны
года объясняется попаданием большого количества органических загрязнений с
поверхностным стоком. Не исключено, что в зимний период процессу аммонификации
препятствует низкая температура.
Концентрации нитритов в
речной воде до сброса очищенных стоков в течение всего года не превышали ПДК, самыми
высокими были летом, минимальными – зимой. После сброса сточных вод уровень
содержания нитритов в природной воде увеличился в 1, 5; 1, 7; 1, 8; 2 раза. Увеличения
содержания нитратов в речной воде не отмечалось, а их количество
соответствовало допустимому уровню как до, так и после сброса в реку очищенных
сточных вод.
Присутствие нитритов и
нитратов в воде может являться признаком промышленного загрязнения. Также
причиной повышенного содержания нитратов и нитритов может служить понижение
температуры, при температуре +9°С снижается скорость нитрификации, при
температуре +6°С процесс прекращается полностью.
Мы считаем, что
присутствие в воде реки минеральных составляющих азота отрицательно сказывается
на развитии и жизнедеятельности гидробионтов, так как нитрификация требует
большего количества кислорода
2NH4+ + ЗО2 = ЗН+ + 2NO2-
+ 2Н2О
Нитраты, попадая в желудочно-кишечный
тракт с питьевой водой и продуктами питания, редуцируют в нитриты, быстро
всасываются в кровь, концентрируясь в эритроцитах, обладают выраженной
способностью окислять гемоглобин эритроцитов с образованием метгемоглобина, не
способного снабжать ткани кислородом, в результате чего развивается гипоксия у
человека и рыб.
Основным лимитирующим
веществом для развития водорослевого «цветения» в водоеме, в большей степени
воздействующим на процесс эвтрофикации, является биогенный элемент фосфор.
Под термином «общий
фосфор» понимают все виды фосфатов, содержащихся в воде - растворимые и
нерастворимые, неорганические и органические соединения фосфора. Установлено, что
достаточно удалить из сточных вод один из основных биогенных элементов (азот и
фосфор) и «цветение» в водоеме, куда сбрасываются эти сточные воды, не
развивается. Поэтому удаление фосфора из сточных вод перед сбросом их в водоемы
является более необходимым, чем удаление азота.
13. Содержание анионов в
речной воде до и после сброса очищенных сточных вод, мг/дм3
|
Показа-
тель
|
До сброса |
После сброса |
ПДК |
| Зима |
Весна |
Лето |
Осень |
Зима |
Весна |
Лето |
Осень |
| Фосфаты |
0, 12
±0, 001
|
0, 18
±0, 002
|
0, 19
±0, 001
|
0, 18
±0, 002
|
0, 260
±0, 010
|
0, 380
±0, 020
|
0, 470
±0, 010
|
0, 360
±0, 010
|
0, 200 |
|
Сульфа-
ты
|
210, 0
±8, 00
|
260, 0
±9, 00
|
280, 0
±7, 10
|
220, 0
±9, 30
|
212, 0
±8, 60
|
261, 00
±10, 10
|
282, 00
±11, 30
|
226, 00
±10, 50
|
500, 00 |
| Хлориды |
167, 1
±10, 2
|
173, 0
±9, 80
|
164, 3
±9, 20
|
180, 1
±10, 4
|
170, 5
±9, 7
|
175, 89
±9, 80
|
168, 9
±8, 50
|
184, 0
±10, 10
|
300, 0 |
Как видно из таблицы 13, содержание
фосфатов в речной воде до сброса очищенных сточных вод соответствовало
допустимым величинам, после сброса – увеличивалось в 2, 2; 2, 1; 2, 5; 2 раза и
превышало ПДК в 1, 3; 1, 9; 2, 4; 1, 8 раза зимой, весной, летом, осенью. Концентрации
сульфатов и хлоридов не превышали ПДК и удерживались на одном уровне до и после
сброса очищенных сточных вод. Максимальный уровень сульфатов установлен в обеих
контролируемых зонах в летний период, хлоридов – в осенний, минимальный – зимой
и летом. Выявленные сезонные изменения связаны с загрязнением речной воды
дождевыми сточными водами, несущими в себе загрязняющие вещества органической
природы.
Подтверждением выше
сказанному являются данные, полученные при определении окисляемости речной воды.
От нее зависит суммарное количество всех углеродсодержащих органических
соединений. Повышенная окисляемость воды указывает на загрязнение источников
водоснабжения органическими веществами.
Результаты определения
окисляемости воды представлены в таблице 14.
Из таблицы видно, что
даже выше места сброса стоков в летний период окисляемость воды в реке высокая
и равна значению 1, 07 ПДК. Это объясняется загрязнением воды поверхностным
стоком во время паводка и дождей. После сброса очищенных сточных вод окисляемость
речной воды повышается зимой на 33; весной на 51; летом на 26; осенью на 27 %.
Следует отметить, что в зимнее время этот показатель фактически равен предельно
допустимому значению, а весной, летом и осенью превышает его на 8, 3; 35 и 8, 4
% соответственно.
14. Окислительные
свойства речной воды, мг О2/дм3
|
Показа-
тель
|
До сброса |
После сброса |
ПДК |
| Зима |
Весна |
Лето |
Осень |
Зима |
Весна |
Лето |
Осень |
|
Перманг. окисля-
емость
|
4, 58
±0, 10
|
5, 02
±0, 20
|
7, 50
±0, 10
|
5, 98
±0, 2
|
6, 09
±0, 20
|
7, 58
±0, 10
|
9, 45
±0, 10
|
7, 59
±0, 20
|
7, 00 |
| БПКполн |
2, 16
±0, 10
|
2, 09
±0, 10
|
1, 75
±0, 10
|
1, 68
±0, 10
|
3, 79
±0, 50
|
3, 65
±0, 10
|
3, 64
±0, 20
|
2, 54
±0, 10
|
2, 00 |
|
Раств.
кислород
|
6, 00
±0, 10
|
6, 20
±0, 20
|
6, 40
±0, 10
|
6, 10
±0, 20
|
5, 70
±0, 20
|
4, 81
±0, 30
|
6, 20
±0, 40
|
6, 00
±0, 20
|
Не <6, 00 |
Исходя из того, что
перманганатная окисляемость является показателем легкоокисляемой органики, можно
полагать, что содержание легкоокисляемых загрязняющих веществ органической
природы в реке достаточно высоко. Однако необходимо учитывать, что среди
загрязняющих веществ имеются органические соединения, которые могут служить
субстратом для микроорганизмов. Поэтому при оценке качества воды используют
такой важный показатель как биохимическое потребление кислорода (БПК).
Как показывают данные
таблицы 14 и рисунка 3, наиболее высокие значения БПКполн установлены в речной воде до сброса стоков зимой и
весной, которые превышали ПДК на 8 и 6, 5 % соответственно, после сброса –
зимой - в 1, 9, весной и летом – в 1, 8 раза, осенью значение этого показателя
снижалось, но все же превышало уровень ПДК на 27 %.
Факт увеличения БПКполн в
весенний и летний периоды можно объяснить поступлением в реку поверхностного
стока. Почвенный покров, богатый органическими веществами, смываемый частично
талыми и ливневыми водами, является источником загрязнения реки органическими
веществами, увеличивающими в воде величину БПКполн. Поэтому факт высокого
значениия БПКполн речной воды в точке выше сброса очищенных сточных вод
объясняется антропогенным загрязнением самих поверхностных вод органическими и
минеральными веществами, смываемыми с несанкционированных свалок на берегу реки,
на окисление которых также расходуется кислород.
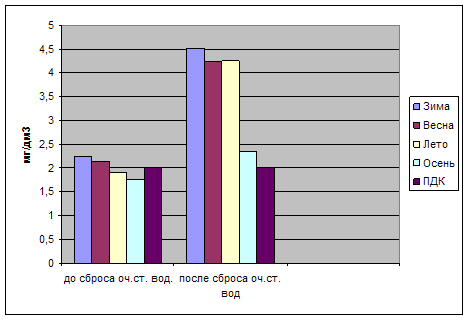
Рис. 3. Сезонная динамика
БПКполн в речной воде до и после сброса очищенных сточных вод
В то же время нельзя
исключать очень важный фактор, существенно влияющий на результат углеводного
БПК - это процесс нитрификации в пробе, значительно увеличивающий потребление
кислорода, которое заметно возрастает после завершения биохимического
разложения углеродсодержащих органических загрязняющих веществ в начале стадии
нитрификации. По этой причине результаты анализа БПКполн могут быть сильно искажены,
что особенно характерно для проб, содержащих нитрифицирующие бактерии и
азотистые загрязнения.
В целом, полученные
данные исследований свидетельствуют, что большое количество кислорода речной
воды расходуется для дыхательной деятельности микроорганизмов, использующих
органическое вещество из исследуемых вод для роста и метаболизма.
Данное предположение
подтверждается снижением уровня содержания растворенного кислорода, по
сравнению с ПДК в речной воде после сброса - зимой – на 5; весной – на 19, 8 %.
Тяжелые металлы - наиболее
распространенная группа токсичных, трудноокисляемых загрязнений, присутствующих
в водах как сточных, так и природных. В водах металлы представлены
разнообразными химическими соединениями во взвешенной, коллоидной, растворенной
и нерастворенной формах.
Катионы металлов по своей
токсичности значительно различаются и по убыванию их можно расположить в следующий
ряд:
Hg2+>Cd2+>Zn2+>Cu2+>Pb2+>Ni2+>Co2+>Sn2+>Ba2+>Fe2+>Mn2+>Sr2+>Mg2+>Ca2+
(Фрумин, 1995).
В процессе биохимической
очистки часть ионов тяжелых металлов аккумулируется илом. Экспериментально
установлены усредненные нормы эффективности удаления некоторых металлов на
сооружениях биологической очистки: Сг - 63-99%, Си - 69-98%, Zn - 44-100%, Ni -
25-74%, Fe - 87-98% (Brown, Lester, 1979).
Нами проведены
исследования по измерению массовой концентрации железа общего, никеля и хрома в
воде реки Сухона до и после сброса в нее очищенных сточных вод.
15. Содержание тяжелых
металлов в речной воде до и после сброса очищенных сточных вод, мг/дм3
|
Показа-
тель
|
До сброса |
После сброса |
ПДК |
| Зима |
Весна |
Лето |
Осень |
Зима |
Весна |
Лето |
Осень |
| Железо общее |
0, 050
±0, 001
|
0, 090
±0, 001
|
0, 170
±0, 001
|
0, 120
±0, 002
|
0, 080
±0, 001
|
0, 100
±0, 040
|
0, 220
±0, 020
|
0, 190
±0, 050
|
0, 100 |
| Никель |
0, 002
±0, 0001
|
0, 001
±0, 0002
|
0, 003
±0, 0001
|
0, 003
±0, 0001
|
0, 003
±0, 0002
|
0, 002
±0, 0001
|
0, 004
±0, 0001
|
0, 004
±0, 0002
|
0, 010 |
| Хром |
0, 003
±0, 0001
|
0, 002
±0, 0001
|
0, 002
±0, 0001
|
0, 002
±0, 0001
|
0, 004
±0, 0001
|
0, 003
±0, 0001
|
0, 003
±0, 0001
|
0, 003
±0, 0001
|
0, 070 |
Результаты исследований
показали, что концентрация железа в пробах воды после превышала ПДК во все
изучаемые периоды, кроме зимнего (таблица 15).
Наиболее высокое
содержание железа общего нами установлено в речной воде до сброса летом - 0, 17
мг/дм3, что выше ПДК в 1, 7 раза, весной и осенью оно несколько снижалось, но
все же было осенью в 1, 2 раза выше ПДК. После сброса очищенных сточных вод во
все периоды значение изучаемого показателя увеличивалось и продолжало превышать
нормативный уровень в 2, 2 раза летом и в 1, 9 раз осенью, весной было равно
ПДК. Железо — один из наиболее распространенных после алюминия компонентов
земной коры (4, 65% по массе): в воде океанов его массовый кларк составляет 0, 000001%,
в биосфере - 0, 0005%. В природных водах его среднее содержание колеблется в
интервале 0, 01-26, 0 мг/л. В большинстве водоемов концентрация железа
составляет до 0, 01 мг/л.
Железо входит в состав
дыхательных белков, поэтому роль его в организме весьма важна. Железо служит
необходимым материалом для синтеза гемоглобина. Этот процесс протекает
нормально при наличии определенных количеств железа, меди и кобальта. Активно
аккумулирует железо водная флора, причем интенсивность накопления зависит от
времени года. Содержание железа в моллюсках значительно зависит от видовых и
региональных различий. Высокие концентрации железа оказывают токсический эффект
на гидробионтов.
Содержание никеля и хрома
в речной воде было ниже допустимых величин во все наблюдаемые периоды (кроме
зимнего) до и после сброса очищенных сточных вод. Самые высокие концентрации
никеля были установлены летом и осенью, хрома – зимой.
Никель относится к редким
элементам, но в отдельных местностях содержание его весьма значительно. Кроме
природных никелевых провинций существуют еще и техногенные. Наиболее токсичными
считают хорошо растворимые хлорид никеля, ацетат никеля, сульфат никеля, наименее
токсичным является металлический никель.
Согласно литературным
данным, токсическое действие хлорида никеля проявляется при концентрации 2, 5
мг/мл воды.
Важным моментом наших
исследований является выявление в речной воде хрома - металла, поступающего в
природные водоемы, в основном, в результате антропогенной деятельности.
В воде встречаются
трехвалентные катионы хрома в составе его сульфатов, хлоридов и нитратов или
шестивалентный хром в виде анионов гидрохромата и хромата. В воде растворяются
хлориды, нитраты и сульфаты хрома, хроматы и бихроматы натрия, калия, аммония.
На рыб хром оказывает кожно-резорбтивное действие.
Помимо специфического
токсического действия ионов хрома, его соединения (хромноватая кислота и
бихроматы) влияют на рыб косвенно, снижая рН воды. С повышением жесткости воды
токсичность соединений хрома снижается.
В связи с тем, что многие
загрязняющие вещества в воде реки Сухона до и после сброса очищенных сточных
вод находились в концентрациях, превышающих ПДК, нами проведена интегральная
оценка водоема (по среднегодовым данным).
С этой целью для расчета
индекса загрязняющих веществ (ИЗВ), нами выбраны следующие показатели: рН, концентрация
взвешенных веществ, содержание растворенного кислорода, БПКполн, перманганатная
окисляемость, концентрация общего железа.
До сброса очищенных
сточных вод ИЗВ составил 1, 34: после сброса - 1, 69.
Согласно полученным
значениям ИЗВ можно сделать заключение, что вода реки Сухона на момент
исследования соответствовала 3 классу качества и характеризовалась как
«умеренно загрязненная».
Таким образом, любые
загрязняющие гидросферу вещества, в том числе и металлы, должны тщательно
исследоваться и оцениваться. При этом необходимо учитывать не только острое, но
и продолжительное или хроническое воздействие загрязняющих веществ и
соответствующие им симптомы интоксикации у людей, животных, рыб и растений.
Выводы
1. Из-за нестабильной
работы МУП «Водоканал» происходит неконтролируемый сброс в реку Сухона сточных
вод, содержащих тяжелые металлы и органические вещества в количествах, превышающих
ПДК.
2. Сточные воды, поступающие
на очистку не соответствуют требованиям СанПиН по прозрачности. Концентрация
фосфатов была выше ПДК в 6, 7 раз, зимой, весной, летом и осенью в 11, 9; 16, 5;
7, 8 раз.
3. Биохимическое
потребление кислорода было в пределах допустимых величин, однако, летом
превышало ПДК в 8, 8 раза.
4. Содержание тяжелых
металлов во все периоды года превышает ПДК: по железу общему – в 1, 2 – 3, 5
раз, по никелю – 1, 7-1, 8 раза, по хрому – на 18-35 %.
5. В сточных водах после
очистки установлены повышенные концентрации некоторых компонентов, которые
превышали предельно допустимые: по взвешенным веществам – в 2, 91, оседающим
веществам – в 2, 21 раз, нитритам – в 2, 25, фосфатам – 7, 4, 3, БПК полн, - 2,
3, железу общему – в 2, никелю – в 1, 5, хрому8, 6 раз.
6. Содержание взвешенных
веществ в речной воде после смешения с очищенными сточными водами превышало ПДК
в 1, 7- 3 раза.
7. Уровень содержания
соединений азота в речной воде после сброса очищенных стоков во все периоды
года был ниже ПДК.
8. Содержание фосфатов в
речной воде после сброса сточных вод превышало ПДК в 1, 3 – 2, 4 раза.
9. Высокие значения
БПКполн установлены в речной воде до сброса стоков, которые превышали ПДК от 27
% до 1, 9 раза.
10. Содержание железа
общего в речной воде после сброса очищенных сточных вод превышало ПДК летом в 2,
2; осенью в 1, 9 раз.
17. Вода реки Сухона на
момент исследования соответствовала 3 классу качества и характеризовалась как
«умеренно загрязненная».
Список литературы
1. Алферова, А.А.
Замкнутые системы водного хозяйства промышленных предприятий, комплексов и
районов. - М.: Стройиздат, 1987.-352 с.
2. Алексеев, Л. С.
Контроль качества воды. - М.: ИНФРА-М, 2004. - 159 с.
3. Бабенков, Е. Н.
Очистка воды коагулянтами. - М.: Наука, 1977. - 137 с.
4. Беспамятнов, Г.П.
Предельно допустимые концентрации химических веществ в окружающей среде. - Л.:
Химия, 1987. - 375 с.
5. Бородатый, И.Т.
Методическое руководство по анализу природных и сточных вод. - Чел.:
Южно-Уральское кн. Изд., 1973. - 178 с.
6. Вронский, В. А.
Экология: Словарь-справочник. - Изд. 2-е. - Ростов н/Д.: Феникс, 2002. - 576с.
7. Голубовская, Э. К. Биологические
основы очистки воды. - М: Высшая школа, 1978.-268 с.
8. Громов, Б.В. Проблемы развития
безотходных производств. - М.: Стройиздат, 1985. - 256 с.
9. Дуганова, Г.В. Охрана
окружающей природной среды. - Киев: Высшая школа, 1990. - 165 с.
10. Евилович, А.З.
Утилизация осадков сточных вод. - М.: Стройиздат, 1989.-158 с.
11. Жуков, А.И. Методы очистки
производственных сточных вод. - М.: Стройиздат, 1988. - 206 с.
12. Жуков, А.И. Методы очистки
производственных сточных вод. - М.: Химия, 1996. - 345 с.
13. Жукова, А. И.
Канализация. - Изд. 4-е. - М.: 1969. - 179 с.
14. Замарин, Е. А.
Гидротехнические сооружения. - М.: Стройиздат, 1965. - 289 с.
15. Ивчатов, А. Л. Химия
воды и микробиология. - М.: ИНФРА-М, 2006.-218 с.
16. Карпинский, А. А.
Новые достижения в технологии сбраживания осадков сточных вод. - М.: Стройиздат,
1959. - 215 с.
17. Кафаров, В.В.
Принципы создания безотходных химических производств. - М.: Химия, 1994. - 276
с.
18. Клепиков, А. И.
Очистка промышленных сточных вод. - Чел.: Челябинская городская типография № 1,
1975.-8 с.
19. Клячко, В. А. Очистка
природных вод. - М.: Стройиздат, 1971. - 176 с.
20. Лурье, Ю. Ю.
Химический анализ производственных сточных вод. - Изд. 3-е. М.: Химия, 1966. - 168
с.
21. Максимовский, Н. С.
Очистка сточных вод. - М.: Стройиздат, 1961. - 193 с.
22. Небел, Б. Наука об
окружающей среде т. 1, М.: Мир, 1993. - 258 с.
23. Петров, К.М. Общая
экология: Взаимодействие общества и природы: Учебное пособие для вузов. - 2-е
изд., стер. - СПб: Химия, 1998. - 352 с.
24. Резников, А. А.
Методы анализа природных вод. - Изд. 2-е. М.: Госгеолтехиздат, 1963. - 149 с.
25. Родзевич, Н. Н.
Геоэкология и природопользование. - М.: Дрофа, 2003.-256 с.
26. СанПиН 2.1.5.980-00.
Гигиенические требования к охране поверхностных вод. - М.: Минздрав, 2001.
27. Соколова, В.Н. Охрана
производственных сточных вод и утилизация осадков. - М.: Стройиздат, 1992. - 259
с.
28. Смирнов, Д. Н.
Очистка сточных вод в процессах обработки металлов. - М.: Металлургия, 1989. - 204
с.
29. Туровский, И.С.
Обработка осадков сточных вод, М.: Стройиздат, 1984. - 163 с.
30. Удаление металлов из
сточных вод. Под редакцией Дж. К. Кушни. - М.: Металлургия, 1987. - 147 с.
31. Юшманова, О.А.
Комплексное использование и охрана водных ресурсов. - М.: Агропромиздат, 1985.
- 328 с.
|