Реферат: Поверхностно-активные вещества. Природные и синтетические. Их преимущества и недостатки
Реферат: Поверхностно-активные вещества. Природные и синтетические. Их преимущества и недостатки
Поверхностно-активные
вещества (ПАВ) — химические соединения, которые, концентрируясь на поверхности
раздела фаз, вызывают снижение поверхностного натяжения.
Основной
количественной характеристикой ПАВ является поверхностная активность —
способность вещества снижать поверхностное натяжение на границе раздела фаз —
это производная поверхностного натяжения по концентрации ПАВ при стремлении С к
нулю. Однако, ПАВ имеет предел растворимости (так называемую критическую
концентрацию мицеллообразования или ККМ), с достижением которого при добавлении
ПАВ в раствор концентрация на границе раздела фаз остается постоянной, но в то
же время происходит самоорганизация молекул ПАВ в объёмном растворе
(мицеллообразование или агрегация). В результате такой агрегации образуются так
называемые мицеллы. Отличительным признаком мицеллообразования служит
помутнение раствора ПАВ. Водные растворы ПАВ, при мицеллообразовании также
приобретают голубоватый оттенок (студенистый оттенок) за счёт преломления света
мицеллами.
Типичные
ПАВ — органические соединения дифильного строения, т. е. содержащие в молекуле
атомные группы, сильно различающиеся по интенсивности взаимодействия с
окружающей средой (в наиболее практически важном случае — водой). Так, в
молекулах ПАВ имеются один или несколько углеводородных радикалов, составляющих
олео-, или липофильную, часть (она же — гидрофобная часть молекулы), и одна или
несколько полярных групп — гидрофильная часть. Слабо взаимодействующие с водой
олеофильные (гидрофобные) группы определяют стремление молекулы к переходу из
водной (полярной) среды в углеводородную (неполярную). Гидрофильные группы,
наоборот, удерживают молекулу в полярной среде или, если молекула ПАВ находится
в углеводородной жидкости, определяют её стремление к переходу в полярную среду.
Т. о., поверхностная активность ПАВ, растворённых в неполярных жидкостях,
обусловлена гидрофильными группами, а растворённых в воде — гидрофобными
радикалами.
Примеры.
По типу гидрофильных групп ПАВ делят на ионные, или ионогенные, и неионные, или
неионогенные. Ионные ПАВ диссоциируют в воде на ионы, одни из которых обладают
адсорбционной (поверхностной) активностью, другие (противоионы) — адсорбционно
неактивны. Если адсорбционно активны анионы, ПАВ называются анионными, или
анионоактивными, в противоположном случае — катионными, или катионо-активными.
Анионные ПАВ — органические кислоты и их соли, катионные — основания, обычно
амины различной степени замещения, и их соли. Некоторые ПАВ содержат и
кислотные, и основные группы. В зависимости от условий они проявляют свойства
или анионных, или катионных ПАВ, поэтому их называют амфотерными, или
амфолитными, ПАВ
Ионогенные ПАВ.
Анионоактивные
вещества составляют большую часть мирового производства ПАВ. Эта группа
тензидов является самой несовместимой с грязью, и именно ее больше всего ругают
мылофобы. Анионные и криптоанионные соединения (ацетилпептиды, лаурил– и
лауретсульфаты натрия, калия, магния или аммония) лучше всех других групп ПАВ
удаляют грязь с контактных поверхностей. Поэтому без них не обходится ни одно
действенное очищающее средство.
Эту
группу моющих субстанций люди научились производить раньше других (вспомним
пассаж про пепел, котором посыпали себе голову древние мудрецы). По мере
развития прогресса анионные тензиды стали варить из белков и жиров, ощелоченных
(натриевая гидролизация) при помощи золы (самое популярное щелочное природное
сырье — зола дерева Salasola soda) и других щелочных соединений. В качестве
сырья для анионных и криптоанионных ПАВ используется кокосовое, пальмовое,
рапсовое, соевое масло, свиной жир, спермацет, масло из коровьего и козьего
молока.
Выдающиеся
очищающие качества анионных тензидов объясняются строением их молекул, которые
состоят из двух частей — гидрофильной (любящей воду) и, наоборот, гидрофобной.
Первые
позволяют им растворяться в воде (или полярных растворителях) и полностью
смываться ею с поверхности кожи, а вторые — контактировать с неполярными
веществами (углеводородами, смолами, мочевиной, пылью, жирами, маслами). Во
время мытья с шампунем или мылом гидрофобные «челюсти» связывают захваченные
частички грязи, помещая их в центр мицеллы (полого шара, образованного рядом
молекул, гидрофильные «хвосты» которых направлены наружу, а внутрь —
гидрофобные «головы»).
Быстрая,
полноценная, качественная эвакуация грязи с поверхности кожи и ее придатков,
пенообразование, бактерицидное (ликвидация грамположительных микроорганизмов) и
бактериостатическое, липолитическое (растворение окисленного жирового секрета
сальных желез и смолисто-минеральных загрязнений кожи) действие.
Промышленные
ПАВ этого типа можно разделить на след. основные группы: карбоновые к-ты и их
соли (мыла), алкилсульфаты (сульфоэфиры), алкилсульфонаты и
алкиларилсульфонаты, прочие продукты.
В
производстве мыл и многих ионо и неионогенных мылоподобных ПАВ используют
карбоновые к-ты, получаемые гидролизом из растительных и животных жиров, и
синтетические жирные к-ты. Промышленное значение имеют также смоляные и жирные
к-ты таллового масла — побочного продукта целлюлозного производства — смоляные
к-ты канифоли, среди которых преобладает абиетиновая.
Наибольшее
значение как ПАВ из солей монокарбоновых к-т имеют мыла (натриевые, калиевые и
аммонийные) жирных к-т RСООН, где R — насыщенный или ненасыщенный нормальный
алифатический радикал с числом атомов углерода 12—18, и мыла (натриевые, реже
калиевые) смоляных к-т. Практическое значение имеют также дикарбоновые к-ты,
напр. алкенилянтарные, получаемые в пром-сти конденсацией непредельных
углеводородов с малеиновым ангидридом.
Алкилсульфаты
синтезируют обычно сульфоэтерификацией высших жирных спиртов или α -
олефинов с последующей нейтрализацией оответственно первичных или вторичных
алкилсерных кислот.
Алкиларилсульфонаты,
гл. обр. моно- и диалкилбензолсульфонаты, а также моно- и
диалкилнафталинсульфонаты составляют больпиую часть синтетич. аняоноактивных
ПАВ.
Алкилсульфонаты
обычно получают из насыщенных углезодородов С12 — С18 нормального строения,
к-рые сульфохлорируют или сульфоокисляют с последующим омылением или
нейтрализацией продукта.
Катионоактивные IIАВ.
Катионные
тензиды — это соединения, которые диссоциируют (растворяются) в водном растворе
с образованием катионов (положительно заряженных молекул).
Четвертичные
аммониевые основания, представляют собой полисахариды, получаемые из молочных
продуктов, ланолина, картофеля, кукурузы, сахарного тростника, свеклы,
подсолнечника.
В
силу своего положительного заряда катионные тензиды притягиваются к
отрицательно заряженным волосам и роговым чешуйкам эпидермиса, ускоряя их
смачивание, фиксируют на их поверхности ценные лечебные компоненты,
содержащиеся в косметическом препарате, а также оказывают брадикиназное
действие (устраняют раздражение, зуд, жжение, отечность). Они захватывают и
удерживают отрицательно заряженные частицы, убивают грамотрицательные бактерии.
Катионные
тензиды — ценные компоненты косметических препаратов (шампуней, бальзамов,
кондиционеров): они активизируют пенообразование, повышают продуктивность
кислородообмена кожи и волос, эмульгируют масляные и ароматические субстанции в
водном растворе, оказывают бактерицидное действие, устраняют остаточный
электрический заряд на волосах после мытья (антистатическое действие),
обеспечивают легкое расчесывание, укладку и повышают КПД лечебных компонентов
на кожу и волосы.
Их
можно разделить на след. основные группы: амины различной степени замещения и
четвертичные аммониевые основания, др. азотсодержащие основания (гуанидиню,
гидрозины, гетероциклические соединении и т. д.), четвертичные фосфониевые и
третичные сульфониевые основания.
Сырьем
для катионоактвных ПАВ, имеющих хозяйственное значение, служат амины,
получаемые из жирных к-т и спиртов, алкгалогенидов, а также алкилфенолов.
Четвертичные аммониевые соли синтезируют из соответствующих длинноцепочечных
галоидных алкилов реакцией с третичными аминами, из аминов хлоралкилированием
или др. путями из синтетических спиртов, фенолов и фенольных смесей.
Большее
значение как катионоактивные ПАВ и как исходные продукты в синтезе неионогенных
ПАВ (см. ниже) имеют не только моно- , но и диамины, полиамины и их
производные.
Амфотерные ПАВ
Производители
качественной косметики для того, чтобы смягчить действие лучших, т.е. анионных
очищающих ингредиентов (в частности, для того чтобы анионные ПАВ не повредили
жировой комплекс гидролипидной мантии) и при этом не снизить ни на йоту
очищающей активности препарата, обязательно вводят в мылящуюся формулу соПАВы.
Амфотерные и неионные тензиды нейтрализуют кислотную реакцию анионов,
способствуют их быстрому расщеплению, при этом увеличивая плотность и уменьшая
«воздушность» (диаметр) пузырьков пены.
Амфотерные
ПАВ являются одним из самых дорогих ингредиентов мылящейся основы. Их получают
выжимкой, экстракцией, настаиванием, ректификацией и окислением природного
сырья (как растительного, так и животного толка). Наиболее известные сырьевые
источники амфотерных тензидов, а именно кокоамфоацетата, лактата,
альфа-аминокислот, пектинов, восков, — это мыльнянка, водоросли, мякоть плодов
яблони, корнеплоды (свекла, морковь, топинамбур), пальмовое масло, молочные
продукты, ланолин.
Даже
элементарные познания в химии дают основания для сомнений в возможности
совмещения в единой формуле катионных и анионных ПАВ, поскольку противоположно
заряженные вещества, попарно притягиваясь друг к другу, уменьшают свое сродство
с водой (выпадают в осадок), и, естественно, снижается очищающая активность.
Только благодаря амфотерным тензидам эта проблема была разрешена: эти
поверхностно-активные вещества благодаря своей способности легко отдавать и
присоединять электронную пару проявляют как кислотные, так и основные свойства
в зависимости от реакции среды, в которой они находятся (так в щелочной среде
они становятся анионами, а в кислотной — катионами).
свойства
амфотерных ПАВ
Амфотерные
тензиды защищают кожу и волосы от сухости и раздражения, реставрируют роговой
слой эпидермиса и кератин волос, смягчают, повышают эластичность соединительной
ткани, придают волосам шелковистость, а пене мылящегося вещества —
кремообразную текстуру.
Получены
из анионоактивных введением в них аминогрупп или из катионоактивных введением
кислотных групп.
Такие
соединения, например RNHCH2CH2COONa получают взаимодействием первичного амина и
метилакрилата с последующим омылением сложноэфирной группы щелочью.
Пром-стью
амфотерные ПАВ выпускаются в небольшом количестве, и их потребление расширяется
медленно.
Неионогенные ПАВ
Соединения,
которые растворяются в воде без образования ионов, называют неионными. Их
группу представляют полигликолевые и полигликоленовые эфиры жирных спиртов
(например, фейстензид — Disodium Laurethsulfosuccinate — текучая жидкость,
состоящая из лимонной кислоты и жирных спиртов). Получают неионные ПАВы
оксиэтилированием растительных масел (касторовое, ростков пшеницы, льна,
кунжута, какао, календулы, петрушки, риса, зверобоя). Неионные ПАВ существуют
только в жидкой или пастообразной форме, поэтому не могут содержаться в твердых
моющих средствах (мыло, порошки).
Водные
растворы сложных эфиров жирных кислот являют собой дисперсионный мицельный
раствор, который часто называют «умным мылом», поскольку он эмульгирует грязь и
жир, удаляя их с поверхности кожи и волос, не повреждая защитную мантию.
Свойства неионных ПАВ
Этот
вид ПАВ привносит моющему средству мягкость, безопасность, экологичность
(биоразлагаемость неионных тензидов составляет 100%). Они стабилизируют мыльную
пену, обладают мягкими свойствами загустителя, оказывают брадикиназное и
полирующее действие, реставрируя наружные слои эпидермиса и волос, способствуют
активизации действия лечебных добавок очищающего препарата.
Это
наиболее перспективный и быстро развивающийся класс ПАВ. Не менее 80—90% таких
ПАВ получают присоединением окиси этилена к спиртам, алкилфенолам, карбоновым
к-там, аминам и др. соединениям с реакционноспособными атомами водорода.
Полиоксиатиленовые эфиры алкилфенолов — самая многочисленная и распространенная
группа неионогенных ПАВ, включающая более сотни торговых названий наиболее
известны препараты ОП-4, ОП-7 и ОП-10. Типичное сырье — октил-, ионил- и
додецилфенолы; кр. того, используют крезолы, крезоловую к-ту, β-нафтол и др.
Если в реакцию взят индивидуальный алкилфенол, готовый продукт представляет
собой смесь ПАВ общей ф-лы RC6H4O(CH2O)mH, где т — степень оксиэтилирования,
зависящая от молярного соотношения исходных компонентов.
Все
ПАВ. можно разделить на две категории по типу систем, образуемых ими при
взаимодействии с растворяющей средой. К одной категории относятся
мицеллообразующие ПАВ. в., к другой — не образующие мицелл. В растворах
мицеллообразующих ПАВ в. выше критической концентрации мицеллообразования (ККМ)
возникают коллоидные частицы (мицеллы), состоящие из десятков или сотен молекул
(ионов). Мицеллы обратимо распадаются на отдельные молекулы или ионы при
разбавлении раствора (точнее, коллоидной дисперсии) до концентрации ниже ККМ.
Таким
образом, растворы мицеллообразующих ПАВ. занимают промежуточное положение между
истинными (молекулярными) и коллоидными растворами, поэтому их часто называют
полуколлоидными системами. К мицеллообразующим ПАВ относят все моющие вещества,
эмульгаторы, смачиватели, диспергаторы и др.
Поверхностную
активность удобно оценивать по наибольшему понижению поверхностного натяжения деленному
на соответствующую концентрацию — ККМ в случае мицеллообразующих ПАВ.
Поверхностная активность обратно пропорциональна ККМ:
Образование
мицелл происходит в узком интервале концентраций, к-рый становится уже и
определенней по мере удлинения гидрофобных радикалов.
Простейшие
мицеллы типичных полуколлоидпых ПАВ, напр. солей жирных к-т, при концентрациях,
не слишком превышающих ККМ, имеют сфероидальную форму.
С
ростом концентрации ПАВ анизометричных мицелл сопровождается резким
возрастанием структурной вязкости, приводящей в нек-рых случаях к
гелеебреаованию, т.е. полной потере текучести.
Действие
детергентов. Мыло известно уже тысячи лет, но только относительно недавно
химики поняли, почему оно обладает моющими свойствами. Механизм удаления грязи
в сущности один и тот же для мыла и синтетических моющих средств. Рассмотрим
его на примере поваренной соли, обычного мыла и алкилбензолсульфоната натрия,
одного из первых синтетических детергентов.
При
растворении в воде поваренная соль диссоциирует на положительно заряженные ионы
натрия и отрицательно заряженные хлорид-ионы. Мыло, т.е. стеарат натрия (I),
сходные с ним вещества, а также алкилбензолсульфонат натрия (II) ведут себя
подобным же образом: они образуют положительно заряженные ионы натрия, но их
отрицательные ионы, в отличие от хлорид-иона, состоят примерно из пятидесяти
атомов.
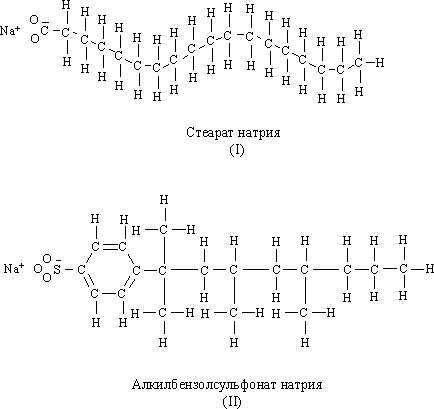
Мыло
(I) можно представить формулой Na+ и C17H35COO–, где 17 атомов углерода с
присоединенными к ним атомами водорода вытянуты в извилистую цепочку.
Алкилбензолсульфонат натрия (Na+ C12H25C6H4SO3–) имеет примерно столько же
атомов углерода и водорода. Однако расположены они не в виде извилистой цепочки,
как в мыле, а в виде разветвленной структуры. Значение этого различия станет
ясно позднее. Для моющего действия важно то, что углеводородная часть
отрицательного иона нерастворима в воде. Однако она растворима в жирах и
маслах, а ведь именно благодаря жиру грязь прилипает к вещам; и если
поверхность полностью очищена от жира, грязь не задерживается на ней.
Отрицательные
ионы (анионы) мыла и алкилбензолсульфоната склонны концентрироваться на
поверхности раздела воды и жира. Водорастворимый отрицательно заряженный конец
остается в воде, тогда как углеводородная часть погружена в жир. Чтобы
поверхность раздела была наибольшей, жир должен присутствовать в виде
мельчайших капелек. В результате образуется эмульсия – взвесь капелек жира
(масла) в воде (III).
Если
на твердой поверхности имеется пленка жира, то при контакте с водой, содержащей
детергент, жир покидает поверхность и переходит в воду в виде мельчайших
капель. Анионы мыла и алкилбензолсульфоната находятся одним концом в воде, а
другим – в жире. Грязь, удерживаемая пленкой жира, удаляется при полоскании.
Так в упрощенном виде можно представить себе действие моющих средств.
Любое
вещество, склонное собираться на поверхности раздела масло – вода, называют
поверхностно-активным веществом. Все поверхностно-активные вещества являются
эмульгаторами, потому что способствуют образованию эмульсии масла в воде, т.е.
«смешению» масла и воды; все они обладают моющими свойствами и образуют пену –
ведь пена является как бы эмульсией воздушных пузырьков в воде. Но не все эти
свойства выражены у них одинаково. Есть поверхностно-активные вещества, которые
обильно образуют пену, но являются слабыми моющими средствами; есть и такие,
которые почти не пенятся, но представляют собой прекрасные моющие средства.
Синтетические детергенты – это синтетические поверхностно-активные вещества с
особо высокой моющей способностью. В промышленности термин «синтетическое
моющее средство», как правило, означает композицию, включающую
поверхностно-активный компонент, отбеливатели и другие добавки.
Мыло,
алкилбензолсульфонаты и многие другие моющие средства, где именно анион
растворяется в жирах, называют анионоактивными. Имеются также
поверхностно-активные вещества, в которых жирорастворимым является катион. Их
называют катионоактивными. Типичный катионный детергент, хлорид
алкилдиметилбензиламмония (IV)

является
солью четвертичного аммония, содержащей азот, связанный с четырьмя группами.
Хлорид-анион всегда остается в воде, поэтому его называют гидрофильным;
углеводородные группы, связанные с положительно заряженным азотом, являются
липофильными. Одна из этих групп, C14H29, похожа на длинную углеводородную
цепочку в мыле и алкилбензолсульфонате, но она присоединена к положительному
иону. Такие вещества называют «обратными мылами». Некоторые из катионоактивных
детергентов обладают сильным антимикробным действием; их применяют в составе
моющих средств, предназначенных не только для мытья, но и для дезинфекции.
Однако если они вызывают раздражение глаз, то при их использовании в
аэрозольных составах это обстоятельство должно быть отражено в инструкции на
этикетке.
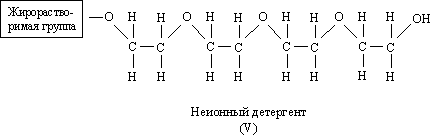
Еще
один тип моющих средств – неионные детергенты. Жирорастворимая группа в
детергенте (V) представляет собой нечто вроде жирорастворимых групп в алкилбензолсульфонатах
и мылах, а остаток – это длинная цепь, содержащая множество кислородных атомов
и OH-группу на конце, которые являются гидрофильными. Обычно неионные
синтетические моющие средства проявляют высокую моющую способность, но слабо
образуют пену.
Раздел
2.
СПАВ
(Синтетические Поверхностно-Активные Вещества) представляют собой обширную
группу соединений, различных по своей структуре, относящихся к разным классам.
Эти вещества способны адсорбироваться на поверхности раздела фаз и понижать
вследствие этого поверхностную энергию (поверхностное натяжение). В зависимости
от свойств, проявляемых СПАВ при растворении в воде, их делят на анионоактивные
вещества (активной частью является анион), катионоактивные (активной частью
молекул является катион), амфолитные и неионогенные, которые совсем не
ионизируются.
Не
секрет, что основные действующие компоненты стиральных порошков -
поверхностно-активные вещества (ПАВ). По правде говоря, эти активные химические
соединения, попадая в организм, разрушают живые клетки путем нарушения
важнейших биохимических процессов.
Будущее
за синтетикой? Видимо, да. В подтверждение этому ПАВ все больше
усовершенствуются, есть так званые неионогенные ПАВ, биоразлагаемость которых
достигает 100%. Они более эффективны при низких температурах, что важно для
щадящих режимов стирки. Поскольку многие искусственные волокна не выдерживают
высоких температур. К тому же стирка в более холодной воде экономит
энергоресурсы, что актуальнее с каждым днем. К сожалению, большинство
неионогенных ПАВ жидкие или пастообразные, и поэтому используются в жидких и
пастообразных моющих средствах. В порошкообразные СМС неионогенные ПАВ вводятся
в виде добавок 2-6%мас. Важные преимущества синтетических ПАВ в том, что они не
образуют малорастворимых в воде солей кальция и магния. А значит, одинаково
хорошо стирают как в мягкой, так и в жесткой вод. Концентрация синтетических
моющих веществ даже в мягкой воде может быть гораздо ниже, чем мыла,
полученного из натуральных жиров.
Наверное,
из продуктов бытовой химии нам известны более всего синтетические моющие
средства. В 1970 году впервые во всем мире синтетических моющих средств (СМС)
было произведено больше, чем обычного натурального мыла. С каждым годом
производство его все снижается, тогда как выпуск СМС непрерывно возрастает.
Например,
в нашей стране динамику роста производства СМС можно отобразить следующими
данными: в 1965 году их было произведено 106 тысяч тонн, в 1970-м—470 тысяч
тонн, а в 1975-м будет выработан почти один миллион тонн.
Почему
же так падает производство натурального, ядрового, мыла, которое верой и
правдой служило человеку долгие годы? Оказывается, у него много недостатков.
Во-первых,
мыло, будучи солью слабой органической кислоты (точнее, солью, образованной
смесью трех кислот— пальмитиновой, маргариновой и стеариновой) и сильного
основания — едкого натра, в воде гидролизует: ся (т. е. расщепляется ею) на
кислоту и щелочь. Кислота вступает в реакцию с солями жесткости и образует
новые, уже нерастворимые в воде соли, которые выпадают в виде клейкой белой
массы на одежду, волосы и т. д. Это не очень приятное явление хорошо известно
всем, кто пытался стирать или мыться в жесткой воде.
Другой
продукт гидролиза — щелочь — разрушает кожу (обезжиривает ее, приводит к
сухости и образованию болезненных трещин) и снижает прочность волокон, из
которых состоят различные ткани. Полиамидные же волокна (капрон, нейлон,
перлон).разрушаются мылом особенно интенсивно.
Во-вторых,
мыло — относительно дорогой продукт, так как для его производства необходимо
пищевое сырье — растительные или животные жиры.
Есть
и другие, менее значительные недостатки у этого до недавнего времени совершенно
незаменимого в быту вещества.
В
отличие от натурального мыла синтетические моющие средства обладают
несомненными достоинствами: большей моющей способностью, гигиеничностью и
экономичностью.
На
международном рынке известно сейчас около 500 наименований синтетических моющих
средств, выпускаемых в виде порошков, гранул, чешуек, паст, жидкостей.
Производство
СМС дает большой народнохозяйственный эффект. Эксперименты показали, что одна
тонна синтетических моющих средств заменяет 1,8 тонны 40°/о-ного хозяйственного
мыла, производимого из ценного пищевого сырья. Подсчитано, что одна тонна СМС
экономит для пищевой промышленности 750 кг растительных жиров.
Применение
СМС в домашнем хозяйстве позволяет сократить затраты труда при ручной и
машинной стирке на 15—20 %• При этом гораздо лучше, чем при использовании
обычного хозяйственного мыла, сохраняются прочность и первоначальные
потребительские свойства ткани (белизна, яркость цвета, эластичность).
Нужно
сказать, что СМС предназначены не только для стирки белья. Есть специальные
средства для мытья и чистки различных предметов домашнего обихода, туалетные
синтетические мыла, средства для мытья волос—шампуни, пеномоющие добавки для
ванн, в которые вводятся биостимуляторы, оказывающие тонизирующее воздействие
на организм.
Главным
компонентом всех названных средств является синтетическое поверхностно-активное
вещество (ПАВ), роль которого та же, что и органической соли в обыкновенном
мыле.
Однако
химикам давно уже известно, что индивидуальное вещество, каким бы универсальным
оно ни было, не может удовлетворять всем предъявляемым к нему требованиям.
Небольшие же добавки других, сопутствующих веществ помогают обнаружить у этого
основного вещества весьма полезные качества. Вот почему все современные СМС
представляют собой не индивидуальные ПАВы, а композиции, в которые могут
входить отбеливатели, отдушки, регуляторы пены, биологически активные вещества
и другие компоненты.
Вторым
по значимости компонентом современных синтетических моющих средств являются
конденсированные, или полимерные, фосфаты (полифосфаты). Эти вещества обладают
рядом полезных свойств: они образуют с имеющимися в воде ионами металлов
водорастворимые комплексы, чем предупреждают возможность появления
нерастворимых минеральных солей, возникающих при стирке обычным мылом;
увеличивают моющую активность ПАВа; предотвращают обратное оседание взвешенных
частиц грязи на отстиранную поверхность; дешевы в производстве.
Все
эти свойства полифосфатов позволяют снизить в СМС содержание более дорогого
основного компонента—ПАВа.
Как
правило, в любое синтетическое моющее средство входит отдушка — вещество с
приятным запахом, который передается белью при использовании СМС.
Почти
во все СМС вводится вещество, называемое натриевой солью
карбоксиметилцеллюлозы. Это — высокомолекулярный синтетический продукт,
растворимый в воде. Его основное предназначение — быть, наряду с фосфатами,
антирезорбтивом, т. е. предотвращать оседание грязи на уже отстиранные волокна.
Большинство
из них имеет ряд преимуществ перед мылом, которое издавна применялись для этой
цели. Так, например, ПАВы хорошо растворяются и пенятся даже в жесткой воде.
Образующиеся в жесткой воде калиевые и магниевые соли не ухудшают моющего
действия ПАВов и не образуют на волосах белого налета.
Основные
действующие вещества всех стиральных порошков, т.н. ПАВ (поверхностно активные
вещества), представляют собой чрезвычайно активные химические соединения.
Обладая некоторым химическим родством с определенными компонентами мембран
клеток человека и животных, ПАВ, при попадании в организм, скапливаются на
клеточных мембранах, покрывая их поверхность тонким слоем и при определенной
концентрации способны вызвать нарушения важнейших биохимических процессов,
протекающих в них, нарушить функцию и саму целостность клетки.
В
экспериментах на животных ученые установили, что ПАВ существенно изменяют интенсивность
окислительно-восстановительных реакций, влияют на активность ряда важнейших
ферментов, нарушают белковый, углеводный и жировой обмен. Особенно агрессивны в
своих действиях анионы ПАВ. Они способны вызвать грубые нарушения иммунитета,
развитие аллергии, поражения мозга, печени, почек, легких. Это одна из причин,
по которым в странах Западной Европы наложены строгие ограничения на
использование а-ПАВ (анионных ПАВ) в составах стиральных порошков. В лучшем
случае их содержание не должно превышать 2-7%. На Западе уже более 10 лет назад
отказались от применения в быту порошков, содержащих фосфатные добавки. На
рынках Германии, Италии, Австрии, Голландии и Норвегии продаются только
бесфосфатные моющие средства. В Германии применение фосфатных порошков
запрещено федеральным законом. В других странах, таких как Франция,
Великобритания, Испания, в соответствии с правительственными решениями
содержание фосфатов в СМС строго регламентировано (не более 12%).
Наличие
фосфатных добавок в порошках приводит к значительному усилению токсических
свойств а-ПАВ. С одной стороны, эти добавки создают условия для более
интенсивного проникновения а-ПАВ через неповрежденную кожу, способствуют
усиленному обезжириванию кожных покровов, более активному разрушению клеточных
мембран, резко снижают барьерную функцию кожи. ПАВ проникают в микрососуды
кожи, всасываются в кровь и распространяются по организму. Это приводит к
изменению физико-химических свойств самой крови и нарушению иммунитета. У а-ПАВ
есть способность накапливаться в органах. Например, в мозге оседает 1,9 %
общего количества а-ПАВ, попавших на незащищенную кожу, в печени - 0,6 % и т.д.
Они действуют подобно ядам: в легких вызывают гиперемию, эмфизему, в печени
повреждают функцию клеток, что приводит к увеличению холестерина и усиливают
явления атеросклероза в сосудах сердца и мозга, нарушает передачу нервных
импульсов в центральной и периферической нервной системах.
Но
этим не исчерпывается вредное действие фосфатов - они представляют собой
большую угрозу для окружающей нас среды. Попадая после стирки вместе со
сточными водами в водоемы, фосфаты принимаются действовать как удобрения.
«Урожай» водорослей в водоемах начинает расти не по дням, а по часам.
Водоросли, разлагаясь, выделяют в огромных количествах метан, аммиак,
сероводород, которые уничтожают все живое в воде. Зарастание водоемов и
засорение медленно текущих вод приводит к грубым нарушениям экосистем водоемов,
ухудшению кислородного обмена в гидросфере и создают трудности в обеспечении
населения питьевой водой. Еще и по этой причине во многих странах
законодательно запретили применение фосфатных СМС.
Традиционным
недостатком ПАВ является жесткость, выражающаяся в раздражении на коже,
появлении сухости и состояния дискомфорта после использования шампуня или геля
для душа.
Кожные
покровы рук, соприкасаясь с активными химическими растворами стиральных
порошков, становятся основным проводником проникновения опасных химических
агентов в организм человека. А-ПАВ активно проникают даже через неповрежденную
кожу рук и при содействии фосфатов, энзимов и хлора интенсивно ее
обеззараживают. Восстановление нормальной жирности и влажности кожи происходит
не ранее, чем через 3-4 часа, а при многократном применении в связи с
накоплением вредного эффекта недостаток жирового покрытия кожи ощущается в
течение двух суток. Барьерные функции кожных покровов снижаются, и создаются
условия для интенсивного проникновения в организм не только а-ПАВ, но и любых
токсичных соединений - бактериологических токсинов, тяжелых металлов и др.
После нескольких стирок фосфатными порошками зачастую развиваются воспаления
кожи - дерматиты. Запускается конвейер патологических иммунных реакций.
Список литературы
Ван
Кревелен Д.В., Свойства и химическое строение полимеров, пер. с англ., М.,1976;
http://provisor.com
http://pharmvestnik.ru
http://darnitsa.ua
http://ru.wikipedia.org/
http://wiki.laser.ru
http://ximicat.com
|